Lantánidos
Los lantanoides (nombre recomendado por la IUPAC) o lantánidos son un grupo de elementos que forman parte del periodo 6 de la tabla periódica de los elementos. Estos elementos son llamados «tierras raras» debido a que se encuentran en forma de óxidos, y también, junto con los actínidos, forman los «elementos de transición interna».
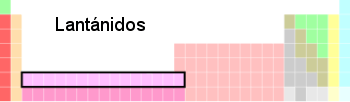
El nombre procede del elemento químico lantano, que suele incluirse dentro de este grupo, dando un total de 15 elementos, desde el de número atómico 57 (el lantano) al 71 (el lutecio).[1][2][3] Aunque se suela incluir en este grupo, el lantano no tiene electrones ocupando ningún orbital f, mientras que los catorce siguientes elementos tienen este orbital 4f parcial o totalmente lleno (véase configuración electrónica).
| N° atómico | Nombre | Símbolo |
|---|---|---|
| 57 | Lantano | La |
| 58 | Cerio | Ce |
| 59 | Praseodimio | Pr |
| 60 | Neodimio | Nd |
| 61 | Prometio | Pm |
| 62 | Samario | Sm |
| 63 | Europio | Eu |
| 64 | Gadolinio | Gd |
| 65 | Terbio | Tb |
| 66 | Disprosio | Dy |
| 67 | Holmio | Ho |
| 68 | Erbio | Er |
| 69 | Tulio | Tm |
| 70 | Iterbio | Yb |
| 71 | Lutecio | Lu |
Estos elementos son químicamente bastante parecidos entre sí puesto que los electrones situados en orbitales f son poco importantes en los enlaces que forman, en comparación con los de p y d. También son bastante parecidos a los lantánidos los elementos itrio y escandio, debido a que tienen un radio similar y, al igual que los lantánidos, su estado de oxidación más importante es el +3. Éste es el estado de oxidación más importante de los lantánidos, pero también presentan el estado de oxidación +2 y +4.
La abundancia de estos elementos en la corteza terrestre es relativamente alta, en minerales como por ejemplo la monacita, en la cual se encuentran distintos lantánidos e itrio.
En la tabla periódica, estos elementos se suelen situar debajo del resto, junto con los actínidos, dando una tabla más compacta que si se colocaran entre los elementos del bloque s y los del bloque d, aunque en algunas tablas periódicas sí que se pueden ver situados entre estos bloques, dando una tabla mucho más ancha.
El radio de los lantánidos va disminuyendo conforme aumenta el número atómico; no son variaciones grandes, pero se van acumulando. Esto provoca que los elementos del bloque d de la segunda y tercera serie de transición presenten radios similares dentro de un grupo: deberían aumentar al bajar en un grupo, pero al haberse intercalado los lantánidos, este aumento en el radio por bajar dentro de un grupo se ve contrarrestado por la disminución del radio por la presencia de los lantánidos. Esto se conoce como contracción de los lantánidos.
Propiedades magnéticas y espectrales
Varios de los aspectos del comportamiento magnético y espectral de los lantánidos difieren fundamentalmente de los del bloque de correspondiente a los elementos de transición. La razón básica de estas diferencias reside en que los electrones que son responsables de las propiedades de los iones lantánidos son electrones 4f, y que los orbitales 4f están protegidos muy efectivamente de la influencia de fuerzas externas en las capas externas 5s2 y 5p6. Es por ello que los estados que se originan desde las diversas configuraciones 4fn sólo son ligeramente afectados por el medio que rodea a los iones y permanecen prácticamente invariables para determinado ion en todos sus compuestos.
Las constantes de acoplamiento de spin-órbita son bastante grandes. Esto tiene por consecuencia que, salvo unas cuantas excepciones, los iones lantánidos posean estados fundamentales con un solo y bien definido valor del momento angular total J, con el siguiente estado inferior de J, y con energías muchas veces mayores que el valor de KT, y por consiguiente el estado superior está virtualmente no poblado.
Los colores y estados electrónicos fundamentales de los iones M3+ se dan en la tabla que se encuentra a continuación; la consecuencia de los colores en la serie del lantano al gadolinio se repiten accidentalmente en la serie del lutecio al gadolinio. Como ha quedado implícito en las explicaciones anteriores, los colores se deben a transiciones f-f , las cuales son virtualmente independientes del entorno exterior de iones.
Véase también
Referencias
- Gray, Theodore (2009). The Elements: A Visual Exploration of Every Known Atom in the Universe. New York: Black Dog & Leventhal Publishers. p. 240. ISBN 978-1-57912-814-2.
- Lanthanide Archivado el 11 de septiembre de 2011 en la Wayback Machine., Encyclopædia Britannica on-line
- Holden, Norman E.; Coplen, Tyler (January–February 2004). «The Periodic Table of the Elements». Chemistry International (IUPAC) 26 (1): 8. doi:10.1515/ci.2004.26.1.8. Archivado desde el original el 17 de febrero de 2004. Consultado el 23 de marzo de 2010.