Arsénico
| Germanio ← Arsénico → Selenio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabla completa • Tabla ampliada | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Información general | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombre, símbolo, número | Arsénico, As, 33 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie química | Metaloides | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 15, 4, p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atómica | 74,922 u | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuración electrónica | [Ar] 3d10 4s2 4p3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Mohs | 3,5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrones por nivel | 2, 8, 18, 5 (imagen) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | Gris metálico | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio medio | 115 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegatividad | 2,0 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico (calc) | 139 pm (radio de Bohr) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | 119 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio de van der Waals | 185 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado(s) de oxidación | ±3,5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Óxido | Levemente ácido | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1.ª energía de ionización | 947,0 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.ª energía de ionización | 1798 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3.ª energía de ionización | 2735 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4.ª energía de ionización | 4837 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5.ª energía de ionización | 6043 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6.ª energía de ionización | 12310 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Líneas espectrales |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado ordinario | Sólido | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad | 5727 kg/m3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de fusión | 887 K (614 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de ebullición | 1090 K (817 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de vaporización | 369,9 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de fusión | 34,76 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varios | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristalina | Romboédrica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor específico | 330 J/(kg·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad eléctrica | 3,45 × 106 S/m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad térmica | 50 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isótopos más estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Artículo principal: Isótopos del arsénico | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Valores en el SI y condiciones normales de presión y temperatura, salvo que se indique lo contrario. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El arsénico es un elemento químico de la tabla periódica que pertenece al grupo de los metaloides, también llamados semimetales. Es un sólido a temperatura ambiente; a presión atmosférica, sublima a 613 °C. Su símbolo es As y el número atómico es 33. En la tabla periódica de los elementos se encuentra en el quinto grupo principal. El arsénico se presenta generalmente en forma de sulfuros. Se conoce desde la antigüedad y es extremadamente tóxico.
Es un elemento esencial para la vida y su deficiencia puede dar lugar a trastornos, pero no se conoce con precisión la función biológica.[1][2][3] La ingesta diaria de hasta 15 μg puede consumirse sin problemas en la dieta diaria en carnes, pescados, vegetales y cereales; siendo los peces y crustáceos los que más contenido de arsénico presentan.
Su nombre proviene del persa zarnikh, ‘oropimente amarillo’.
Se conocen compuestos de arsénico desde la antigüedad, siendo extremadamente tóxicos, aunque se emplean como componentes en algunos medicamentos. Es usado para la fabricación de semiconductores y como componente de semiconductores III-V como el arseniuro de galio.
Es muy común en la atmósfera terrestre, en rocas y suelos, en la hidrosfera y la biosfera. Es llevado al ambiente a través de una combinación de procesos como:
- Naturales como la meteorización, actividad biológica, emisiones volcánicas
- Antropogénicos como la actividad minera, uso de combustibles fósiles, uso de pesticidas, herbicidas, etc.
Características principales
Características físicas

Los tres alótropos de arsénico más comunes son el arsénico gris o metálico, el amarillo y el negro.[4] El arsénico gris (α-As, grupo espacial R3m) es la forma estable en condiciones normales y tiene estructura romboédrica, de doble capa que consiste en muchos anillos entrelazados, ondulados y de seis miembros. Debido a la débil unión entre las capas, el arsénico gris es frágil y tiene una dureza de Mohs relativamente baja de 3,5. Es un buen conductor del calor pero mal conductor eléctrico, su densidad es de 5,73 g/cm³ y pierde el lustre metálico expuesto al aire.[5] El arsénico gris es un semimetal, pero se convierte en un semiconductor con una banda prohibida de 1,2-1,4 eV si se "amorfiza" (se convierte de un material cristalino a uno amorfo).[6]
El arsénico “amarillo” (forma γ) es blando y ceroso y se obtiene cuando el vapor de arsénico se enfría rápidamente. Este alótropo inestable, al ser molecular, es el más volátil, menos denso y más tóxico, además presenta fosforescencia a temperatura ambiente. El gas está constituido por moléculas tetraédricas de As4 de forma análoga al fósforo P4 y el sólido formado por la condensación del gas tiene estructura cúbica y tiene una densidad aproximada de 1,97 g/cm³.[7] Expuesto a la luz o al calor revierte rápidamente a la forma estable (gris). También se denomina arsénico amarillo al oropimente, mineral de trisulfuro de arsénico.
La tercera forma alotrópica, el arsénico “negro” (forma β) de estructura hexagonal y densidad 4,7 g/cm³, tiene propiedades intermedias entre las formas alotrópicas descritas y se obtiene en la descomposición térmica de la arsina o bien enfriando lentamente el vapor de arsénico o por cristalización del arsénico amorfo en presencia de vapores de mercurio.[8] Es vítreo y quebradizo. El arsénico negro también es un mal conductor eléctrico.
Todas las formas alotrópicas excepto la gris carecen de lustre metálico y tienen muy baja conductividad eléctrica por lo que el elemento se comportará como metal o no metal en función, básicamente, de su estado de agregación.[6]
A presión atmosférica el arsénico sublima a 613 °C, y a 400 °C arde con llama blanca formando el sesquióxido As4O6. Reacciona violentamente con el cloro y se combina, al calentarse, con la mayoría de los metales para formar el arseniuro correspondiente. No reacciona con el ácido clorhídrico en ausencia de oxígeno, pero sí con el nítrico caliente, sea diluido o concentrado y otros oxidantes como el peróxido de hidrógeno, ácido perclórico, etc. Es insoluble en agua pero muchos de sus compuestos son solubles.El arsénico sublima al calentarse a presión atmosférica y se convierte directamente en gas sin necesidad de pasar al estado líquido a 887 K (614 °C). El punto triple se encuentra a 3,63 MPa y 1090 K (820 °C).[7]
Isótopos
El arsénico se encuentra en la naturaleza como un isótopo estable, el 75As, y por lo tanto se lo denomina elemento monoisotópico. A partir de 2024, también se han sintetizado al menos 32 radioisótopos, con masas atómicas que van desde 64 hasta 95.[9] El más estable de ellos es el 73As, con una vida media de 80,30 días. Todos los demás isótopos tienen vidas medias inferiores a un día, con la excepción del 71As (t1/2=65,30 horas), el 72As (t1/2=26,0 horas), el 74As (t1/2=17,77 días), el 76As (t1/2=26,26 horas) y el 77As (t1/2=38,83 horas). Los isótopos más ligeros que el estable 75As tienden a desintegrarse por desintegración β+, y los más pesados tienden a desintegrarse por desintegración β−, con algunas excepciones.
Características químicas
El arsénico tiene una electronegatividad y energía de ionización similares a las de su congénere pnictógeno más ligero, el fósforo, y por lo tanto forma fácilmente moléculas covalentes con la mayoría de los no metales. Aunque es estable en aire seco, el arsénico se deslustre formando una capa como de bronce dorado al exponerse a la humedad que finalmente se convierte en una capa superficial negra.[10]
El arsénico reacciona violentamente con agentes oxidantes y halógenos. El arsénico arde en el aire con una llama azulada para producir humo blanco de óxido de arsénico (III) tóxico.
- los vapores de esta reacción tienen un olor parecido al del ajo.
Este olor se puede detectar al golpear minerales de arsénico como la arsenopirita con un martillo. Se quema en oxígeno para formar trióxido de arsénico y pentóxido de arsénico, que tienen la misma estructura que los compuestos de fósforo más conocidos, y reacciona con flúor para dar pentafluoruro de arsénico.
Sin calor externo, la reacción con el cloro se produce con la aparición de fuego para formar cloruro de arsénico(III).
Es posible una mayor oxidación:
Los ácidos oxidantes fuertes, como el ácido nítrico concentrado o el agua regia, convierten el arsénico en ácido arsénico:
Si la fuerza de oxidación es menor, por ejemplo cuando se utiliza ácido nítrico diluido o ácido sulfúrico, se forma ácido arsenioso:
Si se utiliza ácido sulfúrico concentrado, se forma trióxido de arsénico.
Sin embargo, no reacciona con agua, álcalis o ácidos no oxidantes. En condiciones ácidas y en presencia de metales básicos no pasivados, especialmente zinc, el arsénico reacciona con el hidrógeno formado para formar arsano:
- El zinc reacciona con iones de hidrógeno para formar iones de zinc e hidrógeno neutro.
El arsénico reacciona con metales para formar arseniuros, aunque estos no son compuestos iónicos que contengan el ion As3− ya que la formación de dicho anión sería altamente endotérmica e incluso los arseniuros del grupo 1 tienen propiedades de compuestos intermetálicos. Al igual que el germanio, el selenio y el bromo, que como el arsénico sufren la contracción de la serie de transición 3d, el arsénico es mucho menos estable en el estado de oxidación +5 que sus vecinos verticales fósforo y antimonio, y por lo tanto el pentóxido de arsénico y el ácido arsénico son oxidantes potentes.[10]
Compuestos de arsénico
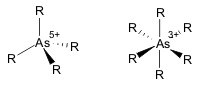
Los compuestos de arsénico se parecen, en algunos aspectos, a los del fósforo, que ocupa el mismo grupo (columna) de la tabla periódica. Los estados de oxidación más comunes del arsénico son: -3 en los arseniuros, que son compuestos intermetálicos similares a aleaciones, +3 en los arsenitos y +5 en los arsenatos y la mayoría de los compuestos organoarsénicos. El arsénico también se enlaza fácilmente consigo mismo, como se ve en los iones cuadrados As3−4 en el mineral escuterudita.[11] En el estado de oxidación +3, el arsénico es típicamente piramidal debido a la influencia del par solitario de electrones.[4]
Compuestos inorgánicos de arsénico
Uno de los compuestos de arsénico más simples es el trihidruro, la arsina pirofórica (AsH3), altamente tóxica e inflamable. Este compuesto generalmente se considera estable, ya que a temperatura ambiente se descompone lentamente. A temperaturas de 250-300 °C, la descomposición en arsénico e hidrógeno es rápida.[10] Varios factores, como la humedad, la presencia de luz y ciertos catalizadores (en particular, el aluminio) facilitan la velocidad de descomposición.[12] Se oxida fácilmente en el aire para formar trióxido de arsénico y agua, y tienen lugar reacciones análogas con azufre y selenio en lugar de oxígeno.[10]
El arsénico forma óxidos cristalinos incoloros e inodoros, As2O3 ("arsénico blanco") y As2O5, que son higroscópicos y fácilmente solubles en agua para formar soluciones ácidas. El ácido arsénico (V) es un ácido débil y sus sales, conocidas como arsenatos,[10] son una fuente importante de contaminación por arsénico de las aguas subterráneas en regiones con altos niveles de minerales de arsénico de origen natural.[13] Los arsenatos sintéticos incluyen el arseniato de calcio y el hidrógeno arseniato de plomo, utilizados como herbicidas, insecticidas y venenos.
Los pasos de protonación entre el arseniato y el ácido arsénico son similares a los que se dan entre el fosfato y el ácido fosfórico. A diferencia del ácido fosforoso, el ácido arsenioso es genuinamente tribásico, con la fórmula As(OH)3.[10]
Se conoce una amplia variedad de compuestos de azufre del arsénico. El oropimente (As2S3) y el rejalgar (As4S4) son bastante abundantes y antiguamente se utilizaban como pigmentos para pinturas. En As4S10, el arsénico tiene un estado de oxidación formal de +2 en As4S4 que presenta enlaces As-As de modo que la covalencia total de As sigue siendo 3.[14] Tanto el oropimente como el rejalgar, así como el As4S3, tienen análogos de selenio; el análogo As2Te3 se conoce como el mineral kalgoorlieíta.[15]
Todos los trihaluros de arsénico(III) son bien conocidos excepto el astaturo, que es desconocido. El pentafluoruro de arsénico (AsF5) es el único pentahaluro importante, lo que refleja la menor estabilidad del estado de oxidación +5; aun así, es un agente fluorante y oxidante muy fuerte. (El pentacloruro es estable solo por debajo de −50 °C, temperatura a la que se descompone en tricloruro, liberando gas cloro).[7]
Compuestos de organoarsénico
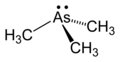
Se conoce una gran variedad de compuestos de organoarsénico. Varios de ellos se desarrollaron como agentes de guerra química durante la Primera Guerra Mundial. El ácido cacodílico, que tiene interés histórico y práctico, surge de la metilación del trióxido de arsénico, una reacción que no tiene analogía en la química del fósforo. El cacodilo fue el primer compuesto organometálico conocido (aunque el arsénico no es un metal verdadero) y recibió su nombre del griego κακωδία "hedor" por su olor ofensivo, parecido al ajo; es muy tóxico.[10]
Historia

El arsénico (del griego άρσενιχόν, oropimente) se conoce desde tiempos remotos, lo mismo que algunos de sus compuestos, especialmente los sulfuros. Dioscórides y Plinio el Viejo (griegos del siglo I) conocían las propiedades del oropimente y el rejalgar y Celso Aureliano (romano del siglo I) y Galeno (siglo II) sabían de sus efectos irritantes, tóxicos, corrosivos y parasiticidas y observaron sus virtudes contra las toses pertinaces, afecciones de la voz y las disneas.
Los médicos árabes usaron también los compuestos de arsénico en fumigaciones, píldoras y pociones además de en aplicaciones externas. Durante la Edad Media los compuestos arsenicales cayeron en el olvido quedando relegados a los curanderos que los prescribían contra la escrófula y el hidrocele.
Roger Bacon y Alberto Magno se detuvieron en su estudio —se cree que este último fue el primero en aislar el elemento en el año 1250— y Paracelso hizo de él una panacea.
El primero que lo estudió con detalle fue George Brandt en 1633, y Johann Schroeder lo obtuvo en 1649 por la acción del carbón sobre el ácido arsénico. A Jöns Jacob Berzelius se deben las primeras investigaciones acerca de la composición de los compuestos del arsénico.
En el siglo XVIII los arsenicales consiguieron un puesto de primer orden en la terapéutica hasta que fueron sustituidos por las sulfamidas y los antibióticos.
Abundancia en la naturaleza

El arsénico se encuentra en bajas concentraciones de hasta 10 ppm prácticamente en todas partes del suelo terrestre. Es tan común en la corteza terrestre como el uranio o el germanio. Así, el arsénico ocupa el puesto 52 en la tabla de elementos más comunes de la corteza terrestre con 2 ppm (5·10−4 %). El arsénico se encuentra en forma nativa y, principalmente, en forma de diversos compuestos intermetálicos con antimonio (alemontita) y cobre (algodonita), así como en diversos minerales, que pertenecen predominantemente a la clase de los sulfuros y las sulfosales, existiendo una gran variedad de minerales que contienen cobre, plomo, hierro (arsenopirita), níquel, cobalto y otros metales.
Las concentraciones más altas de arsénico se encuentran en los minerales duranusita (aprox. 90%), escuterudita y arsenolita (cada uno aproximadamente 76%), que, sin embargo, rara vez se encuentran. Están muy extendidas la arsenopirita (grava de arsénico), la lollingita, el rejalgar y el auripigmento (oropimente). Otros minerales conocidos son la cobaltita, domeikita, enargita, gersdorffita (grava de níquel y arsénico), proustita (plata roja arsénica), rammelsbergita, así como safflorita y sperrylita.
Los arseniatos se encuentran a menudo en rocas que contienen fosfato porque tienen una solubilidad comparable y el mineral de sulfuro más común, la pirita, puede incorporar hasta un pequeño porcentaje de arsénico en masa.
Hoy en día, el arsénico se obtiene como subproducto de la fundición de oro, plata, estaño, cobre, cobalto y otros minerales metálicos no ferrosos, así como en el procesamiento de materias primas de fosfato. Los mayores productores son China, Chile, Marruecos y Perú. El arsénico es poco soluble en agua y, por lo tanto, sólo se encuentra en pequeñas trazas, alrededor de 1,6 ppb (billonésimas de una fracción de masa) en mares y océanos.
Según datos del servicio de prospecciones geológicas estadounidense (U.S. Geological Survey) las minas de cobre y plomo contienen aproximadamente 11 millones de toneladas de arsénico, especialmente en Perú y Filipinas, y el metaloide se encuentra asociado con depósitos de cobre-oro en Chile y de oro en Canadá.
Obtención y síntesis
El arsénico se produce en grandes cantidades como subproducto de la extracción de cobre, plomo, cobalto y oro. En la fusión de estos minerales se obtiene trióxido de arsénico que se volatiliza en el proceso y es arrastrado por los gases de la chimenea que pueden llegar a contener más de una 30 % de trióxido de arsénico. Los gases de la chimenea se refinan posteriormente mezclándolos con pequeñas cantidades de galena o pirita para evitar la formación de arsenitos y por tostación se obtiene trióxido de arsénico entre el 90 y 95 % de pureza, por sublimaciones sucesivas puede obtenerse con una pureza del 99 %.
Reduciendo el óxido con coque (carbón) se obtiene el metaloide, sin embargo la mayoría del arsénico se comercializa como óxido. Prácticamente la totalidad de la producción mundial de arsénico metálico es de China, que es también el mayor productor mundial de trióxido de arsénico.
Calentando pirita de arsénico (FeAsS o FeAs2) en ausencia de aire en tubos de arcilla horizontales, el arsénico elemental se sublima y vuelve a su estado sólido en superficies frías:
- Arsenkies zersetzt sich in Eisensulfid und elementares Arsen.
- La grava arsénica se descompone en arseniuro de hierro y arsénico elemental.
Para la tecnología de semiconductores, el arsénico, cuya pureza debe ser superior al 99,99999%, se produce reduciendo el cloruro de arsénico (III) por destilación múltiple en una corriente de hidrógeno:
- El tricloruro de arsénico reacciona con el hidrógeno para formar cloruro de hidrógeno y arsénico elemental.[16]
Aplicaciones
Agrícolas
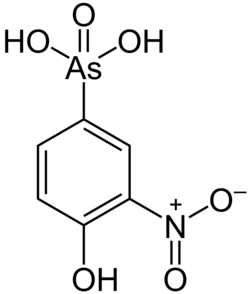
La toxicidad del arsénico para los insectos, las bacterias y los hongos llevó a su uso como conservante de la madera.[17] En la década de 1930, se inventó un proceso de tratamiento de la madera con arseniato de cobre cromado (también conocido como CCA o Tanalith), y durante décadas, este tratamiento fue el uso industrial más extendido del arsénico. Una mayor apreciación de la toxicidad del arsénico llevó a una prohibición del CCA en productos de consumo en 2004, iniciada por la Unión Europea y los Estados Unidos.[18][19] Sin embargo, el CCA sigue siendo de uso intensivo en otros países.[20]
El arsénico también se utilizó en varios insecticidas y venenos agrícolas. Por ejemplo, el arseniato de plomo era un insecticida común en árboles frutales,[21] pero el contacto con el compuesto a veces resultó en daño cerebral entre quienes trabajaban con los pulverizadores. En la segunda mitad del siglo XX, el arseniato de metilo monosódico (MSMA) y el arseniato de metilo disódico (DSMA), formas orgánicas menos tóxicas del arsénico, reemplazaron al arseniato de plomo en la agricultura. Estos arsénicos orgánicos, a su vez, fueron eliminados gradualmente en los Estados Unidos en 2013 en todas las actividades agrícolas, excepto en el cultivo de algodón.[22][23]
La biogeoquímica del arsénico es compleja e incluye varios procesos de adsorción y desorción. La toxicidad del arsénico está relacionada con su solubilidad y se ve afectada por el pH. El arsenito (AsO3−
3) es más soluble que el arseniato (AsO3−
4) y es más tóxico; sin embargo, a un pH más bajo, el arseniato se vuelve más móvil y tóxico. Se descubrió que la adición de azufre, fósforo y óxidos de hierro a suelos con alto contenido de arsenito reduce en gran medida la fitotoxicidad del arsénico.[24]
El arsénico se utiliza como aditivo alimentario en la producción avícola y porcina, en particular se utilizó en los EE. UU. hasta 2015 para aumentar la ganancia de peso, mejorar la eficiencia alimentaria y prevenir enfermedades.[25][26] Un ejemplo es la roxarsona, que había sido utilizada como iniciador de pollos de engorde por aproximadamente el 70% de los criadores de pollos de engorde de EE. UU.[27] En 2011, Alpharma, una subsidiaria de Pfizer, que produce roxarsona, suspendió voluntariamente las ventas del fármaco en respuesta a estudios que mostraban niveles elevados de arsénico inorgánico, un carcinógeno, en pollos tratados.[28] Un sucesor de Alpharma, Zoetis, continuó vendiendo nitarsona hasta 2015, principalmente para su uso en pavos.[28]
Médicas
Durante los siglos XVII, XVIII y XIX, se utilizaron varios compuestos de arsénico como medicamentos, entre ellos la arsfenamina (por Paul Ehrlich) y el trióxido de arsénico (por Thomas Fowler), para tratar enfermedades como el cáncer o la psoriasis.[29] La arsfenamina, así como el neosalvarsan, se indicaban para la sífilis, pero han sido reemplazados por los antibióticos modernos. Sin embargo, los arsénicos como el melarsoprol todavía se utilizan para el tratamiento de la tripanosomiasis, ya que aunque estos fármacos tienen la desventaja de una toxicidad grave, la enfermedad es casi uniformemente mortal si no se trata.[30] En 2000, la Administración de Alimentos y Medicamentos de los Estados Unidos aprobó el trióxido de arsénico para el tratamiento de pacientes con leucemia promielocítica aguda resistente al ácido retinoico all-trans.[31]
Un artículo de 2008 reporta el éxito en la localización de tumores utilizando arsénico-74 (un emisor de positrones). Este isótopo produce imágenes de tomografía por emisión de positrones más claras que el agente radiactivo anterior, el yodo-124, porque el cuerpo tiende a transportar yodo a la glándula tiroides produciendo ruido de señal.[32] Las nanopartículas de arsénico han demostrado la capacidad de matar células cancerosas con menor citotoxicidad que otras formulaciones de arsénico.[33]
Aleaciones
El principal uso del arsénico es en la aleación con plomo. Los componentes de plomo en las baterías de los automóviles se refuerzan con la presencia de un porcentaje muy pequeño de arsénico.[20][34] La descincificación del latón (una aleación de cobre y zinc) se reduce en gran medida con la adición de arsénico.[35] El "cobre arsenical desoxidado con fósforo" con un contenido de arsénico del 0,3 % tiene una mayor estabilidad a la corrosión en ciertos entornos.[36]
El arseniuro de galio es un importante material semiconductor empleado en circuitos integrados más rápidos, y caros, que los de silicio. A diferencia del silicio, el GaAs tiene una banda prohibida directa y se puede utilizar en la construcción de diodos láser y LED.[20]
Militares
Después de la Primera Guerra Mundial, Estados Unidos construyó un arsenal de 20.000 toneladas del compuesto de organoarsénico lewisita (ClCH=CHAsCl2), además de otras sustancias vesicantes e irritantes pulmonares, que fue neutralizado con hipoclorito de sodio y arrojado al Golfo de México en la década de 1950.[37] Durante la Guerra de Vietnam, Estados Unidos utilizó el Agente Azul, una mezcla de ácido cacodílico y su sal sódica, como uno de los herbicidas arco iris para privar a los soldados norvietnamitas de su follaje y arroz.[38][39]
Otros usos
- El disulfuro de arsénico se usa como pigmento y en pirotecnia.
- Decolorante en la fabricación del vidrio (trióxido de arsénico).
- Hasta un 2% del arsénico producido se utiliza en aleaciones de plomo para perdigones y balas de plomo.[40]
- También se utiliza para la conservación de muestras taxonómicas e, históricamente, también se utilizaba en líquidos para embalsamar.
Ya en desuso
- Se ha utilizado para fabricar tintes para tejidos y tintas para imprimir papeles pintados. Esta aplicaciones dieron lugar a graves intoxicaciones en el siglo XIX.[41]
- Se utilizó en el proceso de taxidermia hasta la década de 1980.[42]
- Como elemento fertilizante en forma de mineral primario rico, para la agricultura.
- A lo largo de la historia el arsénico y sus compuestos han sido utilizados con fines homicidas, fundamentalmente en forma de trióxido de diarsénico (polvo blanco, insípido e inodoro llamado rey de los venenos).
Función biológica
La importancia biológica del arsénico para los humanos no se comprende completamente. Se considera un oligoelemento en los seres humanos, pero hasta ahora sólo se han detectado síntomas de deficiencia en animales. El requerimiento necesario, si existe, es de entre 5 y 50 µg por día.[43] Una ingesta diaria de hasta un miligramo de arsénico, dependiendo del alimento que se elija, se considera inofensiva. Si bien el arsénico se asocia con la muerte, es un elemento esencial para la vida y su deficiencia puede dar lugar a diversas complicaciones.[4] La ingesta diaria de 12 a 15 μg puede obtenerse sin problemas con la dieta diaria de carnes, pescados, vegetales y cereales, siendo los peces y crustáceos los que más contenido de arsénico presentan, generalmente en forma de arsenobetaína, menos tóxica que el arsénico inorgánico.
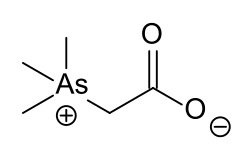
Los animales marinos como los mejillones o los camarones contienen niveles especialmente altos de arsénico, estos últimos hasta 175 ppm. Probablemente actúa como inhibidor uniéndose a los grupos tiol libres de las enzimas, impidiendo así su efecto.
El arsénico es un oligoelemento esencial para muchos animales. Los pollos y ratas que siguen una dieta libre de arsénico muestran importantes trastornos del crecimiento; Probablemente esto esté relacionado con la influencia del elemento sobre el metabolismo del aminoácido arginina. Numerosas algas y crustáceos contienen compuestos orgánicos de arsénico, como la ya mencionada arsenobetaína, además de arsenoazúcares y arsenolípidos. El arsénico conduce a una mayor producción de glóbulos rojos que transportan oxígeno. Por este motivo, anteriormente se añadía a la alimentación de aves y cerdos para permitir un engorde más rápido. Los entrenadores de caballos de carreras lo utilizaban para dopar ilegalmente a sus animales; hoy en día, sin embargo, la adición de arsénico a los alimentos se puede detectar fácilmente en la orina.
Los compuestos solubles de arsénico se absorben fácilmente a través del tracto gastrointestinal y se distribuyen rápidamente por todo el cuerpo en 24 horas. La mayor parte del arsénico absorbido se encuentra en los músculos, huesos, riñones y pulmones. En humanos se ha detectado junto con el talio en casi todos los órganos. La sangre contiene hasta 8 ppb de arsénico, en otros órganos del cuerpo como los huesos tiene una proporción de entre 0,1 y 1,5 ppm, y en el cabello la proporción ronda 1 ppm. De media, la cantidad total de arsénico en el organismo de un adulto ronda los 7 miligramos.
Los compuestos orgánicos de arsénico, como el ácido dimetilarsínico, el óxido de trimetilarsénico, la trimetilarsina y la arsenobetaína, que se encuentran en el pescado y el marisco, abandonan el cuerpo humano casi sin cambios a través de los riñones en dos o tres días. Los compuestos inorgánicos de arsénico se convierten en el hígado en ácido metilarsónico (MMAA) y ácido dimetilarsínico (DMAA) y luego se excretan a través de los riñones.
En las plantas, el elemento aumenta la renovación de carbohidratos. El helecho rayado (Pteris vittata) prefiere absorber el metaloide del suelo y puede absorber hasta el cinco por ciento de su peso seco en arsénico. Por este motivo, esta planta de rápido crecimiento se utiliza para la limpieza biológica de suelos contaminados con arsénico.[44]
El efecto estimulante del arsénico probablemente también sea la razón por la que se consume arsénico, algo muy común en algunas regiones alpinas. En el siglo XVII, algunos de sus habitantes consumían hasta 250 miligramos de arsénico dos veces por semana durante toda su vida: los hombres, porque les ayudaba en el trabajo a gran altura, y las mujeres, porque supuestamente contribuía a tener un cutis fuerte. Descartado durante mucho tiempo por los científicos como un cuento de hadas, en 1875 un granjero de los Alpes de Estiria tomó una dosis de 400 miligramos de trióxido de arsénico delante de los expertos alemanes reunidos en Graz, que luego se detectó en su orina. La dosis era más del doble de la cantidad de arsénico que sería mortal para las personas normales, pero no tuvo efectos negativos en el agricultor. Informes similares han sido hechos por residentes de un asentamiento en el desierto de Atacama chileno, a gran altitud, cuyo agua potable está altamente contaminada con arsénico, pero que no muestran síntomas de envenenamiento. Hoy en día se supone que es fisiológicamente posible acostumbrarse lentamente al veneno con dosis cada vez mayores.
En 2010, la Dra. Felisa Wolfe-Simon del Instituto de Astrobiología de la NASA anunciaba el hallazgo en las aguas tóxicas y salobres del Lago Mono, en California, de una bacteria de la familia Halomonadaceae que podría sustituir el fósforo (que hasta la fecha se consideraba indispensable para la vida) con arsénico, al punto de incorporar este elemento a su ácido desoxirribonucleico (ADN).[45] Este anuncio tuvo gran repercusión en los medios porque, de confirmarse, hubiera abierto la puerta a la búsqueda de nuevas formas de vida en planetas que no contengan fósforo en su atmósfera.[46] Sin embargo, en varios estudios realizados a partir de 2012, la mayoría de las afirmaciones que sostenían el estudio han sido refutadas.[47] Aparentemente, la bacteria sí es resistente al arsénico pero no puede sustituir por completo el fósforo.
Si bien la información anterior fue publicada en la prestigiosa revista científica Science, a la fecha los resultados han y siguen siendo fuertemente cuestionados por numerosos científicos que han tratado de reproducir el mismo diseño experimental sin resultados positivos, a raíz de lo cual han postulado que la bacteria GFAJ-1 pudo sobrevivir en el medio de cultivo sintético empleado para la experimentación gracias a las trazas de fósforo presentes en él.[48]
Precauciones
El arsénico (As) es un metaloide ampliamente distribuido en la naturaleza por causas naturales o antropogénicas. Este elemento se encuentra presente en múltiples formas químicas que difieren en su grado de toxicidad, siendo las formas inorgánicas [arsenito, As(III); arsenato, As(V)] las que producen mayores efectos tóxicos. Por el contrario, especies como la arsenobetaína (AB), la arsenocolina (AC) o el óxido de trimetilarsina (TMAO) se consideran prácticamente inocuas, ya que ninguna de ellas sufre transformaciones tras su absorción. Sin embargo, los ribofuranósidos que contienen arsénico (arsenoazúcares) y los lípidos que contienen arsénico (arsenolípidos), aunque estructuralmente más complejos que otras formas orgánicas, sí sufren transformaciones, dando lugar a formas dimetiladas de mayor toxicidad.[49]
La exposición crónica al arsénico (As) inorgánico a través de la dieta se considera un problema de salud a nivel mundial. Estudios epidemiológicos y mecanísticos han evidenciado su toxicidad en diferentes tipos de células, tejidos u órganos diana. Sólo la exposición a las formas inorgánicas del As se ha asociado a una mayor incidencia de diferentes tipos de cáncer y otros trastornos no cancerosos como la diabetes tipo 2, ciertas enfermedades cardiovasculares o un retraso en el desarrollo neuroconductual en poblaciones expuestas. De hecho, el As inorgánico se considera un carcinógeno humano (tipo 1A) y un potente disruptor endocrino.[49]
Las formas pentavalentes dimetiladas (ácido dimetilarsínico, [DMA(V)] y monometiladas ácido monometilarsónico, [MMA(V)]) han sido consideradas por el IARC como posibles carcinógenos humanos (tipo 2B), basándose en los hallazgos de estudios experimentales en animales. También se ha demostrado una alta toxicidad para sus análogos trivalentes (ácido monometilarsonioso, [MMA(III)]; ácido dimetilarsonioso, [DMA(III)]), siendo estas especies cuya presencia en el agua y los alimentos rara vez se ha documentado, aunque son resultado del metabolismo del As inorgánico.[49]
La mayor parte de la población está expuesta a este metaloide en cualquiera de sus formas, a través de la dieta. Las formas orgánicas se encuentran en productos principalmente de origen marino, donde pueden estar presentes en altas concentraciones. Las formas inorgánicas predominan en alimentos como el arroz, ciertas algas y en productos vegetales.
En Bangladés se ha producido una intoxicación masiva, la mayor de la historia, debido a la construcción de infinidad de pozos de agua promovida por las ONG occidentales que han resultado estar contaminados afectando a una población de cientos de miles de personas.[50] También otras regiones geográficas, España incluida, se han visto afectadas por esta problemática.[51]
Arsénico en el aire
La presencia de arsénico en el aire puede incidir en la prevalencia del cáncer de pulmón. En las fundiciones este elemento es muy común en el aire. Normativas ambientales indican que el máximo permisible es 10 μg/m³.
Arsénico en el agua
La presencia de arsénico en el agua potable puede ser el resultado de la disolución del mineral presente en cuencas hidrográficas cercanas a volcanes y naturalmente en el suelo por donde fluye el agua antes de su captación para uso humano; o bien, por vía antrópica por contaminación industrial o por pesticidas. El arsénico se presenta como As(III) (arsenitos) y As(V) (arseniato, abundante), de los cuales el arsenito es el más tóxico para el humano y el más difícil de remover de los cuerpos de agua. La norma FAO/OMS señala que el nivel máximo permitido se ha reducido a 0,01 ppm o en el agua (anteriormente era de 0,05 ppm).
La ingestión de pequeñas cantidades de arsénico puede causar efectos crónicos por su bioacumulación en el organismo. Envenenamientos graves pueden ocurrir cuando la cantidad tomada es de 100 mg. Se ha atribuido al arsénico enfermedades de prevalencia carcinogénica a la piel, pulmón y vejiga.[52]
Algunos estudios de toxicidad del arsénico indican que muchas de las normas actuales basadas en las guías de la Organización Mundial de la Salud (OMS) señalan concentraciones muy altas y plantean la necesidad de revaluar los valores límites basándose en estudios epidemiológicos.[53]
Normativa en agua
Una manera de ingerir arsénico es a través del agua. Los acuíferos de muchas Comunidades se ven afectados, en estos casos el arsénico generalmente proviene de pozos profundos, donde existe la pirita o arsenopirita (combinación de hierro, azufre y arsénico).
La norma de la Organización Mundial de la Salud (OMS) permite una concentración máxima de arsénico en aguas destinadas para el consumo humano de 10 µg/L. aunque se recomienda no superar los 0,05 mg/L en el agua potable.
Eliminación de arsénico del agua
El tratamiento de agua potable convencional está orientado a eliminar color, turbiedad y microorganismos. Esta eliminación se logra a través de una combinación adecuada de procesos de: coagulación, floculación, sedimentación, filtración y desinfección. Pero cuando se desea eliminar elementos químicos del agua, como el arsénico es necesario, en ocasiones, recurrir a métodos más complejos.
Las tecnologías utilizadas generalmente para eliminar el arsénico, además de coagulación y floculación, son: adsorción-coprecipitación usando sales de hierro y aluminio, adsorción en alúmina activada, ósmosis inversa, intercambio iónico y oxidación seguida de filtración. Otras tecnologías desarrolladas, en lugar de usar sales, emplean un proceso electroquímico que involucra electrodos de latón (Cu2+ and Zn2+) y una fuente de poder que proporciona energía, con lo que se reduce la concentración de arsénico diluido abajo del nivel de detección del espectrofotómetro de absorción atómica.[54]
En las plantas de tratamiento de agua, el As+5 puede ser eliminado en forma efectiva por coagulación con sulfato de aluminio o hierro y por los procesos de ablandamiento con cal. Los coagulantes señalados se hidrolizan formando hidróxidos, sobre los cuales el As+5 se absorbe y coprecipita con otros iones metálicos.[53][55]
Mapas de riesgo de contaminación en aguas subterráneas
Alrededor de un tercio de la población mundial obtiene agua potable de las reservas de agua subterránea. Se estima que alrededor de un 10 por ciento de la población mundial —en torno a 300 millones de personas— se abastecen de agua de reservorios subterráneos contaminados con arsénico y fluoruro. La contaminación por estos oligoelementos es en general de origen natural y se produce por la liberación al medio acuoso de contaminantes por medio de mecanismos de alteración y/o desorción de los minerales contenidos tanto en rocas como en sedimentos.
En el año 2008, el Instituto Suizo de Investigación del Agua (Eawag) presentó un nuevo método que permite establecer mapas de riesgo para sustancias tóxicas de origen geológico en las aguas subterráneas.[56]
Arsénico en el suelo
El arsénico es encontrado de forma natural en la tierra en pequeñas concentraciones, tanto en el suelo como en los minerales, pero también puede entrar en el aire y mucho más fácil en el agua, a través de las tormentas de polvo y las aguas de escorrentía.
Es un componente que difícilmente se convierte en productos solubles en agua o volátiles. Es un elemento muy móvil, refiriéndonos con esto a que grandes concentraciones del mismo no aparecen en un sitio específico, esto tiene aspectos positivos pero también negativos, y es que es por ello por lo que la contaminación por arsénico es amplia debido a la alta movilidad y desplazamiento de este.
Cuando es inmóvil no se puede movilizar fácilmente, pero debido a las actividades humanas (minería y fundición de metales) este arsénico inmóvil se moviliza, ello hace que pueda ser encontrado en lugares donde no existe de forma natural.
Una vez que llega a medio ambiente, este no puede ser destruido, por lo que la cantidad va aumentando y esparciéndose causando efectos sobre la salud de los humanos y los animales.
Efectos en plantas
Las plantas lo absorben fácilmente, ello hace que alto rango de concentraciones pueden estar presentes en la comida (cuando las plantas de consumo humano absorben As).
Tabla I. Contenido de arsénico para un 50 % de reducción del crecimiento
|
Contenido de arsénico para un 50 % de reducción del crecimiento en ppm (Woolson, 1973) | ||
| Tipo de cultivo | Parte comestible | Parte completa |
|---|---|---|
| Rábano (Raphanus sativus) | 76,0 | 43,8 |
| Espinacas (Spinacia oleracea) | 10,0 | 10,0 |
| Repollo (Brassica oleracea) | 1,5 | 3,4 |
| Judías (Phaseolus vulgaris) | 4,2 | 3,7 |
| Tomate (Solanum lycopersicum) | 0,7 | 4,5 |
Efectos en animales
Los peces pueden ver afectado su material genético, ello es debido a la presencia de arsénico inorgánico que antes mencionábamos. Esto es principalmente causado por la acumulación del arsénico en los organismos de las aguas dulces consumidores de plantas.
Las aves también se ven afectadas, sobre todo las que consumen peces con grandes cantidades de arsénico. Mueren como resultado del envenenamiento por arsénico como consecuencia de la descomposición de los peces en sus propios cuerpos.
Efectos en humanos
En humanos la exposición a As es más elevada para aquellos que trabajan en empresas donde utilizan en sus procesos industriales, para gente que vive en casas que contienen conservantes de la madera, gente que vive en granjas donde han sido aplicados pesticidas y herbicidas con As, para personas que usan acuíferos para el suministro de agua que contienen cantidades elevadas de As, como ocurre casi de forma generalizada en algunos países del sur de Asia (India, Tailandia, etc).
Los efectos tóxicos del As en el ser humano dependerá del modo y la duración de la exposición, también será importante la fuente y el tipo de arsénico.
Según algunos estudios la dosis letal de As en adultos será 1-4 mg As/kg[cita requerida] y sus compuestos como AsH3, As2O3, As2O5 la dosis variara entre 1,5 mg/kg y 500 mg/kg de la masa del cuerpo.[cita requerida]
La principal vía de exposición será por ingesta o inhalación, de esta manera entra en el organismo y llega a las superficies epiteliales del tracto digestivo, del aparato respiratorio o de la piel donde se absorbe, entrando en el torrente sanguíneo y siendo transportado a los demás órganos, donde puede ocasionar daños permanentes.
Pasado 24 horas el As puede ser encontrados en hígado, riñón, pulmones, bazo y piel; en la piel se acumula debido a la fácil reacción con las proteínas.
Cuando la ingesta es mayor que la excreción, se acumula en cabello y uñas. El nivel normal de As en la orina es 5-40 µg/día, en el cabello de 80-250 µg/día y en las uñas de 430-1080 µg/día.
Los efectos tóxicos varían dependiendo de varios factores como la genética, la dieta, el metabolismo, a la nutrición entre otras cosas. Los que tienen mayores riesgos son los que tengan una baja metilación del arsénico, los más afectados también serán los niños por su mayor división celular debido a que está en desarrollo y no metabolizará el As como un adulto.
La orina es el mejor bio-marcador para la medición de arsénico inorgánico absorbido, se pueden medir hasta el décimo día después de la exposición. En el cabello o uñas se pueden medir entre los seis a doce meses de la exposición.
Tipos de intoxicación
- Intoxicación aguda
- El arsénico en grandes cantidades afecta la vía digestiva, presentándose como un cuadro gastrointestinal con dolores abdominales, vómitos, diarreas y deshidratación. La pérdida de sensibilidad en el sistema nervioso periférico es el efecto neurológico más frecuente; aparece una a dos semanas después de grandes exposiciones. Los síntomas de la intoxicación aguda pueden aparecer en minutos o bien muchas horas después de la ingestión de entre 100 y 300 mg de As, aunque también es posible la inhalación de polvo de As o la absorción cutánea.
- Intoxicación crónica
- La ingestión de As durante un tiempo prolongado y dosis repetitivas, aparecerán síntomas como: fatiga, gastroenteritis, leucopenia, anemia, hipertensión, alteraciones cutáneas. En la mayoría de los casos los síntomas presentados por intoxicación crónica por arsénico se relacionan a la sintomatología general de algunas enfermedades comunes, debido a esto es necesario realizar un seguimiento del origen de la fuente contaminada por arsénico y una serie de análisis médicos que cuantifiquen la concentración de este en el organismo.
Enfermedades relacionadas
- cáncer de pulmón, vejiga, riñón, próstata
- líneas de Mees
- abortos espontáneos
- malformaciones congénitas
Arsénico en alimentos
El arsénico se encuentra omnipresente en los alimentos, ya que cantidades mínimas del mismo se incorporan por contaminación.
El arsénico puede estar presente en los alimentos por varias causas, estas se muestran en la Tabla II.
Tabla II.
- Principales causas de la presencia de arsénico en los alimentos
Residuos de usos industriales
- Producción de aceros especiales.
- Fabricación de pinturas, vidrio y esmaltes.
Residuos de usos agrícolas y áreas relacionadas
- Herbicidas, fungicidas.
- Insecticidas, rodendicidas.
- Fosfatos que contienen arsénico.
Suplementación mineral de los piensos
Utilización de ácido arsanílico en la alimentación de cerdos y aves de corral para promover su crecimiento.
Residuos de usos farmacéuticos
Utilizado en el tratamiento de enfermedades parasitarias.
Residuos emitidos directamente a la atmósfera
Gases de combustión del carbón y gases industriales.
Los alimentos que llegan al consumidor son producto de una larga cadena de producción, preparación y procesado, durante la cual pueden ser contaminados por elementos metálicos, como por ejemplo de arsénico. Estos elementos se encuentran presentes en toda la biosfera, corteza terrestre, aguas, suelos, atmósfera.
La cantidad de arsénico ingerida por el hombre depende de qué alimentos tome y en qué cantidad, pudiéndose alcanzar contenidos máximos de hasta 40 µg/g.
Véase también
- Semimetal
- James Marsh (químico)
- Intoxicación por arsénico
- Hidropesia
Enlaces y publicaciones originales
- Amini, M.; Mueller, K.; Abbaspour, K.C.; Rosenberg, T.; Afyuni, M.; Møller, M.; Sarr, M.; Johnson, C.A. (2008) «Statistical modeling of global geogenic fluoride contamination in groundwaters.» Environmental Science and Technology, 42(10), 3662-3668, doi:10.1021/es071958y
- Amini, M.; Abbaspour, K. C.; Berg, M.; Winkel, L.; Hug, S. J.; Hoehn, E.; Yang, H.; Johnson, C. A. (2008). «Statistical modeling of global geogenic arsenic contamination in groundwater.» Environmental Science and Technology 42 (10), 3669-3675. doi:10.1021/es702859e
- Winkel, L.; Berg, M.; Amini, M.; Hug, S.J.; Johnson, C.A. «Predicting groundwater arsenic contamination in Southeast Asia from surface parameters.» Nature Geoscience, 1, 536–542 (2008). doi:10.1038/ngeo254
- Rodríguez-Lado, L.; Sun, G.; Berg, M.; Zhang, Q.; Xue, H.; Zheng, Q.; Johnson, C. A. (2013) «Groundwater arsenic contamination throughout China.» Science, 341(6148), 866-868, doi:10.1126/science.1237484 La principal ventaja de esta aproximación, es que permite establecer, para cada zona de extracción, la probabilidad de que el agua esté o no contaminada, lo que facilita los trabajos de muestreo y la identificación de nuevas áreas potencialmente contaminadas.
- En el año 2016 este grupo de investigadores ha puesto a disposición pública los conocimientos adquiridos por medio de la plataforma Groundwater Assessment Platform GAP (www.gapmaps.org). Esta plataforma permite a expertos de todo el mundo, utilizar y visualizar datos analíticos propios, a fin de elaborar mapas de riesgo para una determinada zona de interés. La plataforma GAP funciona al mismo tiempo como un foro de discusión para el intercambio de conocimientos, con el fin de continuar desarrollando y perfeccionando los métodos para la eliminación de sustancias nocivas de las aguas destinadas al consumo humano.
Referencias
- ↑ Anke M. (1986). "Arsenic" (en inglés). p. 347–372. «in Mertz W. (ed.) Trace elements in human and Animal Nutrition, 5ª ed. Orlando, FL: Academic Press».
- ↑ Uthus E.O. (1992). «Evidency for arsenical essentiality». Environ Geochem Health (en inglés) 14: 55-8. PMID 24197927. doi:10.1007/BF01783629.
- ↑ Uthus E.O. (1994). "Arsenic essentiality and factors affecting its importance" (en inglés). pp. 199-208. «in Chappell W.R, Abernathy C.O, Cothern C.R. (eds.) Arsenic Exposure and Health. Northwood, UK: Science and Technology Letters.»
- ↑ a b c Norman, Nicholas C. (1998). Chemistry of Arsenic, Antimony and Bismuth (en inglés). Springer. p. 50. ISBN 978-0-7514-0389-3.
- ↑ Biberg, Egon; Wiberg, Nils; Holleman, Arnold Frederick (2001). Inorganic Chemistry (en inglés). Academic Press. ISBN 978-0-12-352651-9.
- ↑ a b Madelung, Otfried (2004). Semiconductors: data handbook (en inglés). Birkhäuser. pp. 410-. ISBN 978-3-540-40488-0.
- ↑ a b c Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). «Arsen». Lehrbuch der Anorganischen Chemie (en alemán) (91–100 edición). Walter de Gruyter. pp. 675-681. ISBN 3-11-007511-3.
- ↑ Antonatos, Nikolas; Luxa, Jan; Sturala, Jiri; Sofer, Zdeněk (2020). «Black arsenic: a new synthetic method by catalytic crystallization of arsenic glass». Nanoscale (en inglés) 12 (9): 5397-5401. PMID 31894222. S2CID 209544160. doi:10.1039/C9NR09627B.
- ↑ Shimizu, Y.; Kubo, T.; Sumikama, T.; Fukuda, N.; Takeda, H.; Suzuki, H.; Ahn, D. S.; Inabe, N.; Kusaka, K.; Ohtake, M.; Yanagisawa, Y.; Yoshida, K.; Ichikawa, Y.; Isobe, T.; Otsu, H.; Sato, H.; Sonoda, T.; Murai, D.; Iwasa, N.; Imai, N.; Hirayama, Y.; Jeong, S. C.; Kimura, S.; Miyatake, H.; Mukai, M.; Kim, D. G.; Kim, E.; Yagi, A. (8 de abril de 2024). «Production of new neutron-rich isotopes near the N = 60 isotones Ge 92 and As 93 by in-flight fission of a 345 MeV/nucleon U 238 beam». Physical Review C 109 (4): 044313. doi:10.1103/PhysRevC.109.044313.
- ↑ a b c d e f g N.N. Greengood, A. Earnshaw (1997). Chemistry of the Elements. Butterworth-Heinemann. pp. 547-599. ISBN 9780750633659. doi:10.1016/B978-0-7506-3365-9.50019-5.
- ↑ Uher, Ctirad (2001). «Chapter 5 Skutterudites: Prospective novel thermoelectrics». Recent Trends in Thermoelectric Materials Research I: Skutterudites: Prospective novel thermoelectrics. Semiconductors and Semimetals 69. pp. 139-253. ISBN 978-0-12-752178-7. doi:10.1016/S0080-8784(01)80151-4.
- ↑ «Fiche toxicologique No. 53: Trihydrure d'arsenic». Institut National de Recherche et de Sécurité (en francés). 2000. Archivado desde el original el 26 de noviembre de 2006. Consultado el 6 de septiembre de 2006.
- ↑ Smedley, P.L; Kinniburgh, D.G (May 2002). «A review of the source, behaviour and distribution of arsenic in natural waters». Applied Geochemistry 17 (5): 517-568. Bibcode:2002ApGC...17..517S. doi:10.1016/S0883-2927(02)00018-5.
- ↑ «Arsenic: arsenic(II) sulfide compound data». WebElements.com. Archivado desde el original el 11 de diciembre de 2007. Consultado el 10 de diciembre de 2007.
- ↑ «Kalgoorlieite». Mindat. Hudson Institute of Mineralogy. 1993–2017. Consultado el 2 de septiembre de 2017.
- ↑ G. Brauer (Hrsg.): Handbook of Preparative Inorganic Chemistry. 2. Auflage. vol. 1, Academic Press 1963, S. 591–592.
- ↑ Rahman, F. A.; Allan, D. L.; Rosen, C. J.; Sadowsky, M. J. (2004). «Arsenic availability from chromated copper arsenate (CCA)-treated wood». Journal of Environmental Quality 33 (1): 173-180. PMID 14964372. doi:10.2134/jeq2004.0173.
- ↑ Lichtfouse, Eric (2004). «Electrodialytical Removal of Cu, Cr and As from Threaded Wood». En Lichtfouse, Eric; Schwarzbauer, Jan; Robert, Didier, eds. Environmental Chemistry: Green Chemistry and Pollutants in Ecosystems. Berlin: Springer. ISBN 978-3-540-22860-8.
- ↑ Mandal, Badal Kumar; Suzuki, K. T. (2002). «Arsenic round the world: a review». Talanta 58 (1): 201-235. PMID 18968746. doi:10.1016/S0039-9140(02)00268-0.
- ↑ a b c Grund, Sabina C.; Hanusch, Kunibert; Wolf, Hans Uwe. Arsenic and Arsenic Compounds (en inglés). doi:10.1002/14356007.a03_113.pub2.
- ↑ Peryea, F. J. (20–26 August 1998). Historical use of lead arsenate insecticides, resulting in soil contamination and implications for soil remediation. 16th World Congress of Soil Science. Montpellier, France. Archivado desde el original el 7 de diciembre de 2008.
- ↑ «Organic Arsenicals; Notice of Receipt of Requests to Voluntarily Cancel or to Amend to Terminate Uses of Certain Pesticide Registrations». Federal Register. Government Printing Office. Consultado el 18 de julio de 2023.
- ↑ «Monosodium Methanearsonate (MSMA), an Organic Arsenical». Environmental Protection Agency. 22 de abril de 2015. Consultado el 18 de julio de 2023.
- ↑ «Trace Elements in Soils and Plants, Third Edition». CRC Press. Archivado desde el original el 21 de agosto de 2016. Consultado el 2 de agosto de 2016.
- ↑ Nachman, Keeve E.; Graham, Jay P.; Price, Lance B.; Silbergeld, Ellen K. (2005). «Arsenic: A Roadblock to Potential Animal Waste Management Solutions». Environmental Health Perspectives 113 (9): 1123-1124. PMC 1280389. PMID 16140615. doi:10.1289/ehp.7834.
- ↑ «Arsenic». Agency for Toxic Substances and Disease Registry. Section 5.3, p. 310. Archivado desde el original el 9 de octubre de 2022.
- ↑ Jones, F. T. (2007). «A Broad View of Arsenic». Poultry Science 86 (1): 2-14. PMID 17179408. doi:10.1093/ps/86.1.2.
- ↑ a b Staff (8 de junio de 2011). «Questions and Answers Regarding 3-Nitro (Roxarsone)». U.S. Food and Drug Administration. Consultado el 21 de septiembre de 2012.
- ↑ Gibaud, Stéphane; Jaouen, Gérard (2010). «Arsenic - based drugs: from Fowler’s solution to modern anticancer chemotherapy». Topics in Organometallic Chemistry (en inglés) 32: 1-20. doi:10.1007/978-3-642-13185-1_1.
- ↑ Büscher P, Cecchi G, Jamonneau V, Priotto G (2017). «Human African trypanosomiasis». Lancet 390 (10110): 2397-2409. PMID 28673422. S2CID 4853616. doi:10.1016/S0140-6736(17)31510-6.
- ↑ Antman, Karen H. (2001). «The History of Arsenic Trioxide in Cancer Therapy». The Oncologist 6 (Suppl 2): 1-2. PMID 11331433. doi:10.1634/theoncologist.6-suppl_2-1.
- ↑ Jennewein, Marc; Lewis, M. A.; Zhao, D.; Tsyganov, E.; Slavine, N.; He, J.; Watkins, L.; Kodibagkar, V. D.; O'Kelly, S.; Kulkarni, P.; Antich, P.; Hermanne, A.; Rösch, F.; Mason, R.; Thorpe, Ph. (2008). «Vascular Imaging of Solid Tumors in Rats with a Radioactive Arsenic-Labeled Antibody that Binds Exposed Phosphatidylserine». Clinical Cancer Research 14 (5): 1377-1385. PMC 3436070. PMID 18316558. doi:10.1158/1078-0432.CCR-07-1516.
- ↑ Subastri, Ariraman; Arun, Viswanathan; Sharma, Preeti; Preedia babu, Ezhuthupurakkal; Suyavaran, Arumugam; Nithyananthan, Subramaniyam; Alshammari, Ghedeir M.; Aristatile, Balakrishnan; Dharuman, Venkataraman; Thirunavukkarasu, Chinnasamy (November 2018). «Synthesis and characterisation of arsenic nanoparticles and its interaction with DNA and cytotoxic potential on breast cancer cells». Chemico-Biological Interactions 295: 73-83. Bibcode:2018CBI...295...73S. PMID 29277637. S2CID 1816043. doi:10.1016/j.cbi.2017.12.025.
- ↑ Bagshaw, N. E. (1995). «Lead alloys: Past, present and future». Journal of Power Sources 53 (1): 25-30. Bibcode:1995JPS....53...25B. doi:10.1016/0378-7753(94)01973-Y.
- ↑ Joseph, Günter; Kundig, Konrad J. A; Association, International Copper (1999). «Dealloying». Copper: Its Trade, Manufacture, Use, and Environmental Status. ASM International. pp. 123-124. ISBN 978-0-87170-656-0.
- ↑ Nayar (1997). The Metals Databook. McGraw-Hill. p. 6. ISBN 978-0-07-462300-8.
- ↑ «Blister Agents». Code Red – Weapons of Mass Destruction. Consultado el 15 de mayo de 2010.
- ↑ Westing, Arthur H. (1972). «Herbicides in war: Current status and future doubt». Biological Conservation 4 (5): 322-327. Bibcode:1972BCons...4..322W. doi:10.1016/0006-3207(72)90043-2.
- ↑ Westing, Arthur H. (1971). «Forestry and the War in South Vietnam». Journal of Forestry 69: 777-783.
- ↑ Guruswamy, Sivaraman (1999). «XIV. Ammunition». Engineering Properties and Applications of Lead Alloys. CRC Press. pp. 569-570. ISBN 978-0-8247-8247-4.
- ↑ Calvo Sevillano, Guiomar (2021). Historia del arsénico. Guadalmazán. ISBN 978-84-17547-35-6.
- ↑ Marte, Fernando; Pequignot, Amandine (2006). «Arsenic in Taxidermy Collections: History, Detection, and Management». Collection Forum 21 (1–2): 143-150. hdl:10088/8134.
- ↑ John Emsley: Parfum, Portwein, PVC …. Wiley Verlag, Weinheim 2003, S. 274–275.
- ↑ Fei Zhao, Yu Han, Hongyi Shi, Guoxiang Wang, Mingxi Zhou, Yanshan Chen (2023). Arsenic in the hyperaccumulator Pteris vittata: A review of benefits, toxicity, and metabolism. Science of The Total Environment. doi:10.1016/j.scitotenv.2023.165232.
- ↑ Wolfe-Simon, F.; Blum, J. S.; Kulp, T. R.; Gordon, G. W.; Hoeft, S. E.; Pett-Ridge, J.; Stolz, J. F.; Webb, S. M.; Weber, P. K.; Davies, P. C. W.; Anbar, A. D.; Oremland, R. S. (2010). «A Bacterium That Can Grow by Using Arsenic Instead of Phosphorus». Science 332 (6034): 1163-1166. Bibcode:2011Sci...332.1163W. PMID 21127214. doi:10.1126/science.1197258.
- ↑ «La NASA encuentra una nueva forma de vida en la Tierra». La Voz de Galicia. 2 de diciembre de 2010. Consultado el 22 de agosto de 2017.
- ↑ BBC News, ed. (9 de julio de 2012). «Studies refute arsenic bug claim.» (en inglés).
- ↑ Hayden, E. C. (3 de junio de 2011). Nature 474:19, ed. ««Will you take these “arsenic-life” test?»» (en inglés).
- ↑ a b c A. Domene, P. Rodríguez-Viso, A. Sánchez, L. Burbano, H. Orozco, D. Vélez, V. Devesa (2023). «10 - Arsenic through the gastrointestinal tract». Handbook of Arsenic Toxicology (Second Edition): 303-326. ISBN 9780323898478. doi:10.1016/B978-0-323-89847-8.00009-2.
- ↑ Andrew Meharg (2005). Macmillan Science, ed. Venomous Earth - How Arsenic Caused The World's Worst Mass Poisoning. ISBN 9781403944993.
- ↑ Martín-Gil, J.; San Martín Toro, J. M.; y Martín-Villota, M. J. (2002). Tecnoambiente, año XII (118), p. 5-9, ed. «Problemática planteada por la presencia de niveles elevados de arsénico en el Acuífero de Los Arenales (sur del Duero)».
- ↑ OMS, ed. (febrero de 2018). «Cancer» (en inglés).
- ↑ a b «Remoción de Arsénico». Consultado el 10 de octubre de 2012.
- ↑
- ↑ «Normativa para el Arsénico ATSDR». Archivado desde el original el 8 de julio de 2007.
- ↑ Eawag (2015). C.A. Johnson, A. Bretzler (coordinadores), Swiss Federal Institute of Aquatic Science and Technology (Eawag), ed. Geogenic Contamination Handbook – Addressing Arsenic and Fluoride in Drinking Water (en inglés). Duebendorf, Suiza.
Enlaces externos
 Wikimedia Commons alberga una categoría multimedia sobre Arsénico.
Wikimedia Commons alberga una categoría multimedia sobre Arsénico.- ATSDR en Español - Resumen de Salud Pública: Arsénico: Departamento de Salud y Servicios Humanos de EE. UU. (dominio público).
- ATSDR en Español - ToxFAQs™: Arsénico: Departamento de Salud y Servicios Humanos de EE. UU. (dominio público).
- Los Alamos National Laboratory. Arsenic.
- ATSDR en Español - Exposición total al arsénico: Estudio de un caso práctico. Departamento de Salud y Servicios Humanos de EE. UU.
- Efectos del arsénico sobre la salud. Resumen realizado por GreenFacts de un informe de la OMS.
- Enciclopedia Libre. Arsénico.
- EnvironmentalChemistry.com - Arsenic.
- James B. Calvert. Arsénico.
- U.S. Geological Survey - Arsénico.
- WebElements.com - Arsenic.
_NIST_ASD_emission_spectrum.png)