Oro
| Platino ← Oro → Mercurio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabla completa • Tabla ampliada | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Información general | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombre, símbolo, número | Oro, Au, 79 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie química | Metales de transición | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 11, 6, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atómica | 196,966569(4) u | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuración electrónica | [Xe] 4f14 5d10 6s1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Mohs | 3,0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrones por nivel | 2, 8, 18, 32, 18, 1 (imagen) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | Amarillo metálico | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio medio | 135 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegatividad | 2,54 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico (calc) | 173 pm (radio de Bohr) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | 144 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio de van der Waals | 166 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado(s) de oxidación | 3, 1 (anfótero) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1.ª energía de ionización | 890,1 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.ª energía de ionización | 1980 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Líneas espectrales |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado ordinario | Sólido | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad | 19 300 kg/m3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de fusión | 1337,33 K (1064 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de ebullición | 3129 K (2856 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de vaporización | 3,097 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de fusión | 12,55 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presión de vapor | 0,000237 Pa a 1337 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varios | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristalina | cúbica centrada en las caras | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor específico | 128 J/(kg·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad eléctrica | 4,5 × 107 S/m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad térmica | 317 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidad del sonido | 1.740 m/s a 293,15 K (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isótopos más estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Artículo principal: Isótopos del oro | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Valores en el SI y condiciones normales de presión y temperatura, salvo que se indique lo contrario. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El oro es un elemento químico cuyo número atómico es 79. Está ubicado en el grupo 11 de la tabla periódica. Es un metal precioso blando de color amarillo dorado. Su símbolo es Au (del latín aurum, ‘brillante amanecer’). Además, es uno de los metales más apreciados en joyería por sus propiedades físicas, al tener baja alterabilidad, ser muy maleable, dúctil y brillante, y valorado por su rareza, al ser un metal difícil de encontrar en la naturaleza.
Es un metal de transición blando, brillante, amarillo, pesado, maleable y dúctil. El oro no reacciona con la mayoría de los productos químicos, pero es sensible y soluble al cianuro, al mercurio, al agua regia, al cloro y a la lejía. Este metal se encuentra normalmente en estado puro, en forma de pepitas y depósitos aluviales. Es un elemento que se crea gracias a las condiciones extremas en el núcleo colapsante de las supernovas. Cuando la reacción de una fusión nuclear cesa, las capas superiores de la estrella se desploman sobre el núcleo estelar, comprimiendo y calentando la materia hasta el punto de que los núcleos más ligeros, como por ejemplo el hierro, se fusionan para dar lugar a los metales más pesados (uranio, oro, etc.). Un estudio sugiere que el oro del planeta provino de la colisión de estrellas de neutrones.[1]
Los depósitos primarios de oro en la corteza se forman a partir de gases y líquidos muy calientes, metasomáticos, que se elevan desde el interior de la Tierra, los cuales se trasladan a la superficie a través de fallas de la corteza terrestre.[2]
En heráldica, representa todo poder económico y es símbolo de vanidad.
Propiedades
_4_(16848647509).jpg)

El oro exhibe un color amarillo en bruto. Es considerado como el metal más maleable y dúctil que se conoce.[2] Una onza troy (31,10 g aproximadamente) de oro puede moldearse en una lámina que cubra 28 m².[cita requerida] Como es un metal blando, son frecuentes las aleaciones con otros metales con el fin de proporcionarle dureza.
Además, es un buen conductor del calor y de la electricidad, y no le afecta el aire ni la mayoría de los agentes químicos. Tiene una alta resistencia a la alteración química por parte del calor, la humedad y la mayoría de los agentes corrosivos, y así está bien adaptado a su uso en la acuñación de monedas y en la joyería.
Se trata de un metal muy denso, con un alto punto de fusión y una alta afinidad electrónica. Sus estados de oxidación más importantes son 1+ y 3+. También se encuentra en el estado de oxidación 2+, así como en estados de oxidación superiores, pero es menos frecuente. La estabilidad de especies y compuestos de oro con estado de oxidación III, frente a sus homólogos de grupo, hay que razonarla considerando los efectos relativistas sobre los orbitales 5d del oro.
La química del oro es más diversa que la de la plata, su vecino inmediato de grupo: seis estados de oxidación exhibe –I a III y V. El oro –I y V no tiene contrapartida en la química de la plata. Los efectos relativistas, contracción del orbital 6s, hacen al oro diferente con relación a los elementos más ligeros de su grupo: formación de interacciones Au-Au en complejos polinucleares. Las diferencias entre Ag y Au hay que buscarlas en los efectos relativistas que se ejercen sobre los electrones 5d y 6s del oro. El radio covalente de la tríada de su grupo sigue la tendencia Cu < Ag >- Au; el oro tiene un radio covalente ligeramente menor o igual al de la plata en compuestos similares, lo que podemos asignar al fenómeno conocido como “contracción relativista + contracción lantánida”.
Electrones solvatados en amoniaco líquido reducen al oro a Au-. En la serie de compuestos MAu (M: Na, K, Rb, Cs) se debilita el carácter metálico desde Na a Cs. El CsAu es un semiconductor con estructura CsCl y se describe mejor como compuesto iónico: Cs+Au-. Hay que resaltar los compuestos iónicos del oro del tipo RbAu y CsAu con estructura tipo CsCl (8:8), ya que se alcanza la configuración tipo pseudogás noble del Hg (de 6s1 a 6s²) para el ion Au- (contracción lantánida + contracción relativista máxima en los elementos Au y Hg). El subnivel 6s se acerca mucho más al núcleo y simultáneamente el 6p se separa por su expansión relativista. Con esto se justifica el comportamiento noble de estos metales. La afinidad electrónica del Au, –222,7 kJ mol−1, es comparable a la del yodo con –295,3 kJ mol−1. Recientemente se han caracterizado óxidos (M+)3Au-O2-(M = Rb, Cs) que también exhiben propiedades semiconductoras.
Reactividad
El oro es sumamente inactivo. Es inalterable por el aire, el calor, la humedad y la mayoría de los agentes químicos, aunque se disuelve en mezclas que contienen cloruros, bromuros o yoduro. También se disuelve en otras mezclas oxidantes, en cianuros alcalinos y en agua regia, una mezcla de ácido nítrico y ácido clorhídrico. Una vez disuelto en agua regia, se obtiene ácido cloroáurico, que se puede transformar en oro metal con disulfito de sodio. El oro se vuelve soluble al estar expuesto al cianuro.
Isótopos
El oro solo tiene un isótopo estable,197Au, el cual es también su único isótopo de origen natural. 36 radioisótopos han sido sintetizados variando en masa atómica entre 169 y 205. El más estable de estos es 195Au con un periodo de semidesintegración de 186,1 días. 195Au es también el único isótopo que se desintegra por captura electrónica. El menos estable es 171Au, el cual se desintegra por emisión de protones con un periodo de semidesintegración de 30 µs. La mayoría de radioisótopos del oro con masas atómicas por debajo de 197 se desintegran por alguna combinación de emisión de protones, desintegración α y desintegración β+. Las excepciones son 195Au, el cual se desintegra por captura electrónica, y 196Au, el cual tiene un camino de desintegración β- menor. Todos los radioisótopos del oro con masas atómicas por encima de 197 se desintegran por desintegración β-.[3]
Por lo menos 32 isómeros nucleares han sido también caracterizados, variando en masa atómica entre 170 y 200. Dentro de este rango, solo 178Au, 180Au, 181Au, 182Au y 188Au no tienen isómeros. El isómero más estable del oro es 198 m²Au con un periodo de semidesintegración de 2,27 días. El isómero menos estable del oro es 177 m²Au con un periodo de semidesintegración de solo 7 ns. 184 m1Au tiene tres caminos de desintegración: desintegración β+, transición isomérica y desintegración alfa. Ningún otro isómero o isótopo del oro tiene tres caminos de desintegración.[3]
Compuestos
_chloride_solution.jpg)
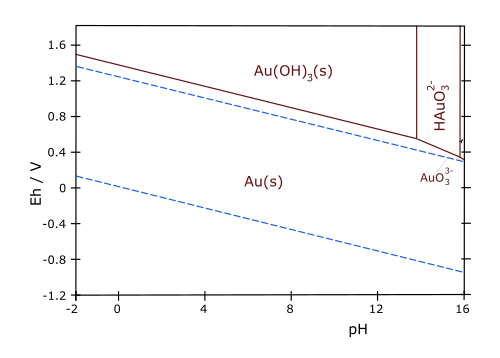
No existe evidencia del estado de oxidación IV, pero si para el Au(V) en el fluoruro AuF5 (rojo oscuro, d>60C, inestable, polimérico y diamagnético;su estructura consiste en octaedros AuF6 unidos por los vértices, generando un polímero monodimensional) y en el anión complejo [AuF6]- (oxidante fuerte, el más fuerte de las especies metálicas [MF6]-, donde tenemos una configuración de bajo espín d6).
El oro forma bastantes complejos pero pocos compuestos sencillos. No se ha aislado un óxido con Au(I), pero si el AuO que contiene Au+ y Au3+, pero el estado I solo es estable en estado sólido o en forma de complejos estables como el anión lineal [Au(CN)2]-, ya que en disolución se desproporciona en oro y oro(III).
El óxido Au2O3 se obtiene, como precipitado amorfo, Au2O3.nH2O, de color marrón, en medio alcalino a partir del halurocomplejo planocuadrado [AuCl4]-. El Au2O3 cristalino, polímero monodimensional, se obtiene mejor por vía hidrotermal y su estructura se genera con grupos planocuadrados [AuO4] unidos por vértices; es poco estable, como es de esperar, y descompone en Au y O2 a 150 °C.
La cloración de polvo de oro a 200 °C da moléculas diméricas planas de Au2Cl6, rojo (d>160 °C), que es el reactivo de partida para preparar muchos compuestos de oro; cuando se calienta a 160 °C produce el AuCl. Se conocen los tres monohaluros AuX (X = Cl, Br, I) cuya estructura se define por cadenas en zig-zag,...X-Au-X..., con puentes angulares Au-X-Au (72°-90°).
El ion dicianoaurato [Au(CN)2]- de gran importancia metalúrgica se forma con facilidad cuando se hace reaccionar oro con disoluciones de cianuros en presencia de aire o agua oxigenada. El Au(III) es d8 e isoelectrónico con Pt(II), teniendo sus complejos preferencia por la geometría plana cuadrada. La disolución de oro en agua regia o de Au2O3 en ácido clorhídrico concentrado nos da el ion tetracloroaurato(III), [AuCl4]-, que se usa como “oro líquido” para decorar cerámicas y vidrios, ya que cuando se calienta deja una película de oro. La evaporación de estas disoluciones producen cristales amarillos de (H3O)[AuCl4].3H2O; las disoluciones acuosas de esta sal generan un medio fuertemente ácido. Este anión tetracloroaurato(III),[AuCl4]-, se hidroliza fácilmente a [AuCl3OH]-.
El “tricloruro de oro” (Au2Cl6) y el “ácido cloroáurico” ((H3O)[AuCl4].3H2O) son algunos de los compuestos más comunes de oro.
También existen otros aniones planocuadrados del tipo [AuX4]-, siendo X: F-,Cl-, Br-, I-, CN-, SCN- y NO3-; este último es uno de los pocos ejemplos auténticos donde el ion nitrato actúa como ligando monodentado, al igual que en los complejos equivalentes de Pd(II) y Pt(II).
Por otro lado se conocen cationes complejos con amoniaco, aminas, piridina y con ligandos quelatos como etilendiamina: [Au(NH3)4]3+ y [AuCl2(py)2]+. En el complejo [Au Cl2 (en)2]+ aparece una coordinación rara para el Au(III) en un entorno octaédrico distorsionado.
La mayoría de los compuestos que se cree que contienen oro(II) en realidad son compuestos de valencia mixta, como el dicloruro de oro que en realidad es el tetrámero (AuI)2(AuIII)2Cl8 donde aparece Au(III) planocuadrado y Au(I) lineal y su color oscuro se origina por la transferencia de carga entre ambos centros metálicos.
También forma cúmulos de oro (compuestos clúster), aspecto desconocido en la química del cobre, su homólogo de grupo más ligero. En este tipo de compuestos hay enlaces entre los átomos de oro que están favorecidos por los efectos relativistas. A algunos de estos compuestos se les denomina “oro líquido”. El clúster trimetálico más voluminoso caracterizado por difracción de rayos-X corresponde al macroanión,[(Ph3P)10 Au12Ag12PtCl7]-, en cuya formación juega un rol importante el oro. Este contiene 25 átomos de elementos vecinos del bloque d y sin participación de metales ligeros de la primera serie de transición: 12Au + 12Ag + 1Pt. Esta clase de clúster queda definida estructuralmente por dos icosaedros Au6Ag6 unidos por un vértice común de oro, situándose en el centro de un icosaedro un átomo de platino y en el segundo el atómo central es de oro.
Historia

El oro ha sido conocido y utilizado por los artesanos desde el Calcolítico. Artefactos de oro fabricados desde el IV milenio a. C., como los provenientes de la necrópolis de Varna (primer oro trabajado del mundo[4]), han sido encontrados en los Balcanes. Otros artefactos de oro, como los sombreros de oro y el disco de Nebra, aparecieron en Europa Central desde el II milenio a. C. en la Edad del Bronce. El oro se conoce desde la prehistoria. En el Antiguo Egipto, el faraón Dyer (3000 a. C.) llevaba en su título un jeroglífico referente al metal, y también se menciona varias veces en el Antiguo Testamento. Se ha considerado uno de los metales más preciosos a lo largo de la Historia, y como "valor patrón" se ha empleado profusamente, acuñado en monedas.
En la antigüedad algunos creían que ingerir sus alimentos diarios servidos en platos de oro podría prolongar su tiempo de vida y retardar el envejecimiento. También durante la gran peste negra en Europa algunos alquimistas pensaron que podrían curar a los enfermos haciéndoles ingerir oro finamente pulverizado.
De manera independiente, el oro también fue trabajado en la América precolombina a mano de la Cultura zapoteca y el Antiguo Perú desde la cultura Chavín de Huántar. Estos pueblos utilizaron el oro con fines ornamentales y ceremoniales. Según las crónicas escritas de Bernal Díaz del Castillo "La verdadera historia de la conquista de la Nueva España" los Aztecas poseían un cuarto secreto del palacio de Axayácatl repleto de esculturas y armas hechas principalmente de oro. Los conquistadores decidieron tomar dichas riquezas para la producción de lingotes, pero en la calzada que salía de Tenochtitlan fueron descubiertos, causando indignación en la ciudad que desembocó en la Noche Triste.

Por otra parte, los Incas poseían grandes cantidades de oro en sus palacios y templos de Cusco,[5] ya que asociaban el material con el sol Inti, la deidad patrona del imperio. Algunos textos de conquistadores como Pedro Cieza de León y sus crónicas Conquista del Tahuantinsuyo afirman que en el Coricancha existía una habitación que contenía paredes, esculturas y utensilios hechos completamente de oro, además de un jardín con llamas, árboles y animales autóctonos en tamaño real hechos de este metal. Cuando los conquistadores capturaron al emperador inca Atahualpa, éste prometió llenar una habitación completamente de oro a cambio de su libertad. Esto se cumplió, pero aun así, los españoles terminaron por ejecutarlo debido a que su liberación podía suponer un gran obstáculo en la conquista del Perú.[6][7] Son de referencia internacional el Tumi de oro de Lambayeque hallado en 1936 y la Máscara Sicán hallado en la época de 1990.[8][9]
Los Muiscas de la actual Colombia son conocidos por rendir culto al oro. Algunos testigos afirmaban que los gobernantes de la confederación se reunían en un lago donde se cubrían con polvo de oro. Estos avistamientos posiblemente fueron la base para evolucionar en la leyenda de El Dorado.
Aplicaciones



De la producción mundial de oro el 70 % se utiliza en joyería, el 20 % en reservas e inversiones y solo al 10 % se le da usos industriales.[10]
El oro puro o de 24 kt (quilates) es demasiado blando para ser usado normalmente y se endurece aleándolo con plata y/o cobre, con lo cual podrá tener distintos tonos de color o matices. El oro y sus muchas aleaciones se emplean bastante en joyería, en relación con el intercambio monetario (para la fabricación de monedas y como patrón monetario), como mercancía, en medicina, en alimentos y bebidas, en la industria, en electrónica y en química comercial.

El oro se conoce y se aprecia desde tiempos remotos, no solamente por su belleza y resistencia a la corrosión, sino también por ser más fácil de trabajar que otros metales y menos costosa su extracción. Debido a su relativa rareza, comenzó a usarse como moneda de cambio y como referencia en las transacciones monetarias internacionales. Hoy por hoy, los países emplean reservas de oro puro en lingotes que dan cuenta de su riqueza, véase patrón oro.
En joyería fina se denomina oro alto o de 18 kt aquel que tiene 18 partes de oro y 6 de otro metal o metales (75 % en oro), oro medio o de 14 kt al que tiene 14 partes de oro y 10 de otros metales (58,33 % en oro) y oro bajo o de 10 kt al que tiene 10 partes de oro por 14 de otros metales (41,67 % en oro). En joyería, el oro de 18 kt es muy brillante y vistoso, pero es caro y poco resistente al desgaste; el oro medio es el de más amplio uso en joyería, ya que es menos caro que el oro de 18 kt y más resistente al desgaste por las aleaciones que contiene, y el oro de 10 kt es el más simple. Debido a su buena conductividad eléctrica y resistencia a la corrosión, así como una buena combinación de propiedades químicas y físicas, se comenzó a emplear a finales del siglo XX como metal en la industria.
En joyería se utilizan diferentes aleaciones de oro alto para obtener diferentes colores, a saber:
- Oro azul = 75% de oro y 25% de hierro.
- Oro gris = 75% de oro, 15% de níquel y 10% de cobre.
- Oro rojo = 75% de oro y 25% de cobre.
- Oro rosa = 75% de oro, 5% de plata y 20% de cobre.
- Oro amarillo = 75% de oro, 12,5% de plata y 12,5% de cobre.
- Oro verde = 75% de oro y 25% de plata.
- Oro blanco = 75% de oro, 16% de paladio y 9% de plata.
Cabe mencionar que el color que se obtiene, excepto en oro blanco, es predominantemente amarillo, es decir, el “oro verde” no es verde, sino amarillo con una tonalidad verdosa.
Medicina
En la actualidad se le ha dado algunos usos terapéuticos: algunos tiolatos (o parecidos) de oro (I) se emplean como antiinflamatorios en el tratamiento de la artritis reumatoide y otras enfermedades reumáticas.[11] No se conoce bien el funcionamiento de estas sales de oro. El uso de oro en medicina es conocido como crisoterapia.
La mayoría de estos compuestos son poco solubles y es necesario inyectarlos. Algunos son más solubles y se pueden administrar por vía oral. Este tratamiento suele presentar bastantes efectos secundarios, generalmente leves, pero es la principal causa de que los pacientes lo abandonen.
El cuerpo humano no absorbe bien este metal, pero sus compuestos pueden ser tóxicos. Hasta el 50 % de pacientes con artrosis tratados con medicamentos que contenían oro han sufrido daños hepáticos y renales.
Más recientemente se han estudiado las nanopartículas de oro dentro del campo médico. Estas pueden ser utilizadas en sensor, imaginería médica, transporte de medicamentos e incluso en terapia fototérmica.
Oro como valor especulativo
- El oro es utilizado como cobertura contra el dólar, la inflación, tasas de interés y crisis económicas. Algunos tenedores de oro lo almacenan en forma de lingotes o monedas con finalidad especulativa. Sin embargo, el economista Martin Feldstein no cree que el oro sirva como una cobertura contra la inflación o depreciación de la moneda. En cambio otros economistas, como Baur, Lucey o Hillier, opinan que el oro no solo sirve como cobertura, sino que sirve como valor refugio durante las crisis económicas.[12]
- El código ISO 4217 de la moneda de oro es XAU.
- Las modernas monedas de oro con fines de inversión, colección o especulación no requieren buenas propiedades de desgaste mecánico; por lo general son de oro fino en 24 kt, aunque el American Gold Eagle y el británico Soberano de Oro continúan siendo acuñados en metal de 22 kt en la tradición histórica; y el sudafricano Krugerrand, mostrado en público por primera vez en 1967, también es 22 kt. El ejemplar especial de la moneda canadiense Hoja de Arce de Oro tiene la pureza de oro más alta de cualquier moneda de oro, el 99,999 % o 0,99999, mientras que el ejemplar popular de la moneda de oro canadiense Hoja de Arce de Oro tiene una pureza un poco inferior, de 99,99 %.
- Hay otras monedas de oro puro al 99,99 % disponibles. En 2006, la Casa de Moneda de los Estados Unidos comenzó la producción de la moneda de oro American Buffalo con una pureza del 99,99 %. La moneda de oro australiana Canguros de Oro (Gold Kangaroos) se acuñó por primera vez en 1986 como Nugget australiano de oro, pero cambió el diseño del reverso en 1989. Otras monedas populares modernas son la moneda de oro Filarmónica de Viena y el Panda de Oro Chino.
Otras aplicaciones
- El oro ejerce funciones críticas en comunicaciones, naves espaciales, motores de aviones de reacción y otros muchos productos.
- Su alta conductividad eléctrica y su resistencia a la oxidación han permitido un amplio uso como capas delgadas electrodepositadas sobre la superficie de conexiones eléctricas para asegurar una conexión buena, de baja resistencia.
- Como la plata, el oro puede formar fuertes amalgamas con el mercurio que a veces se emplean en empastes dentales.
- El oro coloidal (nanopartículas de oro) es una solución intensamente coloreada que se está estudiando en muchos laboratorios con fines médicos y biológicos.[cita requerida] También es la forma empleada como pintura dorada en cerámicas.
- El ácido cloroáurico se emplea en fotografía.
- El isótopo de oro 198Au, con un periodo de semidesintegración de 2,7 días, se emplea en algunos tratamientos de cáncer y de otras enfermedades.
- Se emplea como recubrimiento de materiales biológicos que puede mirarse a través del microscopio electrónico de barrido (SEM).
- Se emplea como recubrimiento protector en muchos satélites debido a que es un buen reflector de la luz infrarroja.
- En la mayoría de las competencias deportivas se entrega una medalla de oro al/a la deportista del primer lugar, una de plata a la del segundo lugar y una de bronce a la del tercer lugar.
- Se ha iniciado su uso en cremas faciales o para la piel.
- Se utiliza para la elaboración de flautas traveseras finas, debido a que se calienta con mayor rapidez que otros materiales, lo que facilita la interpretación del instrumento.
- Se usó en los primeros cables eléctricos en vez del cobre, debido a su gran conductividad eléctrica. Sin embargo, se sustituyó por la plata, debido a que se producían robos, lo que también condujo a la decisión de sustituir la plata por cobre.[cita requerida]
Minería


Debido a que es relativamente inerte, se suele encontrar como metal, a veces como pepitas grandes, pero generalmente se encuentra en pequeñas inclusiones en algunos minerales, vetas de cuarzo, pizarra, rocas metamórficas y depósitos aluviales originados de estas fuentes. El oro está ampliamente distribuido y a menudo se encuentra asociado a los minerales cuarzo y pirita, y se combina con teluro en los minerales calaverita, silvanita y otros. Los romanos extraían mucho oro de Hispania, pero hoy en día muchas de las minas están agotadas.
El oro se extrae por lixiviación con cianuro. El uso del cianuro facilita la oxidación del oro formándose Au (CN)22- en la disolución. Para separar el oro se vuelve a reducir empleando, por ejemplo, zinc. Se ha intentado reemplazar el cianuro por algún otro ligando debido a los problemas medioambientales que genera, pero o no son rentables o también son tóxicos. En la actualidad hay miles de comunidades en todo el mundo en lucha contra compañías mineras por la defensa de sus formas de vida tradicionales y contra los impactos sociales, económicos y medioambientales que la actividad minera de extracción de oro por lixiviación con cianuro genera en su entorno.
Hay una gran cantidad de oro en los mares y océanos, siendo su concentración de entre 0,1 µg/kg y 2 µg/kg, pero en este caso no hay ningún método rentable para obtenerlo.
El oro puede encontrarse en la naturaleza en los ríos. Algunas piedras de los ríos contienen pepitas de oro en su interior. La fuerza del agua separa las pepitas de la roca y las divide en partículas minúsculas que se depositan en el fondo del cauce.
Los buscadores de oro localizan estas partículas de oro de los ríos mediante la técnica del bateo. El utensilio utilizado es la batea, un recipiente con forma de sartén. La batea se llena con arena y agua del río y se va moviendo provocando que los materiales de mayor peso, como el oro, sean depositados en el fondo y la arena superficial se desprenda.
Así pues, el bateo de oro es una técnica de separación de mezclas heterogéneas.
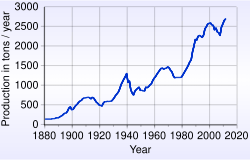
Producción minera
La producción mundial de oro durante el 2014 alcanzó un total de 2860 toneladas métricas de oro fino. El principal país productor fue China, seguido por Australia y Rusia.
| País | Producción minera | Reservas | Base de reservas | |
|---|---|---|---|---|
| 2019 | 2020 [15] | |||
| 380 | 380 | 2000 | - | |
| 325 | 320 | 10000 | - | |
| 305 | 300 | 7500 | - | |
| 200 | 190 | 3000 | - | |
| 175 | 170 | 2200 | - | |
| 142 | 140 | 1000 | - | |
| 139 | 130 | 2600 | - | |
| 128 | 120 | 2700 | - | |
| 111 | 100 | 1400 | - | |
| 107 | 100 | 1000 | - | |
| 105 | 90 | 2700 | - | |
| 90 | 80 | 2400 | - | |
| Otros países | 716 | 750 | 9200 | - |
| Total mundo (redondeado) | 3300 | 3200 | 53000 | - |
Países exportadores
Los principales países exportadores de oro a nivel mundial en 2019 son Suiza, Australia, Reino Unido, Emiratos Árabes Unidos y Sudáfrica.[16]
| N.º | País/Región | Valor de Exportación (en dólares) |
|---|---|---|
| - | Mundo | USD 308.000 millones |
| 1 | USD 65.300 millones | |
| 2 | USD 41.600 millones | |
| 3 | USD 40.800 millones | |
| 4 | USD 15.800 millones | |
| 5 | USD 13.400 millones | |
| 6 | USD 12.500 millones | |
| 7 | USD 10.000 millones | |
| 8 | USD 8.450 millones | |
| 9 | USD 5.740 millones | |
| 10 | USD 5.670 millones |
Forma parte del grupo de minerales de conflicto llamado 3TG, compuesto por la casiterita, la wolframita, el coltán y el oro. Este grupo de minerales es más conocido por las siglas en inglés de sus metales derivados más utilizados: tin (estaño), tungsten (tungsteno), tantalio (tántalo) y gold (oro). Tanto los minerales como los metales derivados son recursos críticos para las industrias como la electrónica, la automotriz o la aviación; y son regulados por legislaciones de alcance internacional como la ley estadounidense Dodd Frank (sección 1502) o la Regulación de los Minerales de Conflicto de la UE debido a que en numerosas ocasiones estos minerales se extraen en zonas de conflicto y sirven para financiar y perpetuar estos conflictos.[17][18][19]
Ensayos
El método de ensayo a fuego consiste en producir una fusión de la muestra usando reactivos fundentes adecuados para obtener dos fases líquidas: una escoria constituida principalmente por silicatos complejos y una fase metálica constituida por plomo, el cual colecta los metales nobles de interés (Au y Ag). Los dos líquidos se separan en dos fases debido a su respectiva inmiscibilidad y gran diferencia de densidad, estos solidifican al enfriar. El plomo sólido (con los metales nobles colectados) es separado de la escoria como un régulo. Este régulo de plomo obtenido es oxidado en caliente en copela de magnesita y absorbido por ella, quedando en su superficie el botón de oro y plata, elementos que se determinan posteriormente por método gravimétrico (por peso) o mediante espectroscopia de absorción atómica.
Toxicidad
Algunos medicamentos como el tiosulfato de oro, la aurotioglucosa, el tiomalato de sodio y oro (miocrisine), etc.; pueden provocar un cuadro de intoxicación por oro. Produciendo efectos adversos como exantemas cutáneos, erupciones papulosas, herpes simple y dermatitis exfoliativa grave. En el sistema digestivo, estos fármacos pueden causar salivación, gusto metálico, náuseas, vómito y diarrea, apareciendo hepatosis y nefritis. En el sistema nervioso puede aparecer anemia aplástica, granulocitopenia y púrpura trombocitopénica. El tratamiento consiste en suspender la medicación, administrar dimercaprol por vía intramuscular y tratar los síntomas.[20]

En la cultura popular
El oro ha tenido mucha referencia en sentido figurado en el habla y cultura populares, por ejemplo:
- La regla de oro que refiere a ciertas normas humanas y luego ha sido tomada en varias disciplinas científicas, con un significado particular en cada una de ellas.
- Cuando se califica algo como valioso o apreciado se dice que es “de oro”.
- “Oro negro” se refiere al petróleo, por ser riqueza natural no renovable a nivel mundial.
- “Oro rosa” puede referirse a los camarones, por ser medio de subsistencia de quienes explotan su captura.
- “Oro verde” es otro nombre con el que se conoce al henequén en Yucatán, al aguacate en Michoacán, a las esmeraldas en Colombia, a la planta de coca en Perú, al cannabis y a la soja.
- “Oro blanco” es el calificativo frecuentemente adjudicado al platino y en otras ocasiones al clorhidrato de cocaína. También se le conoce al algodón por los campesinos que se dedican a su cultivo, además del marfil que se obtiene ilegalmente de los colmillos de los elefantes. También se le denomina oro blanco al litio cuando aparece en reservas grandes en algunas partes del mundo.[21]
- “Oro rojo” se llama al coral rojo (Corallium rubrum) por los artesanos y joyeros que trabajan con él para hacer diversas manufacturas y ornatos. Este coral es un pólipo que forma colonias poco ramificadas de hasta 20 cm. Los pólipos son de color blanco y la estructura que los une es roja. Se encuentra a partir de 15 metros de profundidad. Por otro lado, también “oro rojo” es el calificativo que se utiliza en el bajo mundo para referirse a la sangre humana traficada ilegalmente. También se lo denomina al cobre rojo.
- “Oro líquido” se conoce al aceite de oliva, por la similitud de color entre estas dos sustancias.
- El miedo irracional al oro es la crisofobia, que no hay que confundir con su variante, la aurantrofobia (fobia al dinero).
- No todo lo que brilla es oro, como proverbio.
- El oro no es un elemento esencial para ningún ser vivo. Sin embargo, en la antigüedad algunos creían que ingerir sus alimentos diarios servidos en platos de oro podría prolongar su tiempo de vida y retardar el envejecimiento. También durante la gran peste negra en Europa algunos alquimistas pensaron que podrían curar a los enfermos haciéndoles ingerir oro finamente pulverizado.[cita requerida]
- El oro laminado es una lámina de oro que se ha aplicado a un metal de menor valor.[22]
- El oro de plástico o tarjeta de Crédito Gold. De hasta U$S 30.000 dólares o $ 7.000.000 de pesos en Crédito bancario. Algunas tarjetas vienen doradas o bañadas en oro.
El valor del oro en la historia
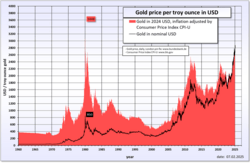
- Su uso especulativo ha creado una burbuja de oro[23] que estalló el 16 de abril de 2013, que fue una jornada histórica en la que el precio de la onza se desplomó un 9 %, el mayor descenso en un solo día desde 1983 (el mayor en 30 años), pero en dos sesiones ha bajado un 13,5 %, con lo que el precio de la onza quedó en 1351 dólares. En lo que va de año 2013, acumula bajadas de casi un 20 % (19,5 %).[24]
- Tras el mínimo de noviembre de 2013, en el que se alcanzó la cifra de 1187 dólares por cada onza de oro, un mínimo que no se alcanzaba desde 2010, el año 2014 empezó con una dinámica positiva que colocó el precio del oro por encima de los 1400 dólares apenas llegados a febrero de 2014, un aumento del 24 % muy importante en los primeros meses de 2014. a partir de abril comenzó un paulatino descenso durante diciembre de 2015 llegó a un mínimo histórico de 1180 dólares la onza, inició un leve ascenso durante 2016 y 2019 entre un rango variable de 1200 y 1400 dólares la onza. a partir de 2019 inició un ascenso que no ha parado hasta agosto de 2020[25][26]
- El martes 4 de agosto de 2020, los precios del oro alcanzaron los 2000 dólares la onza por primera vez en la historia, al ser visto como un activo refugio en medio de la incertidumbre económica causada por la crisis del COVID-19.[2] Para el cierre del año 2020 el precio del oro quedó en 1893.84 dólares la onza.[27]
- Para marzo de 2021 el precio de la onza de oro marcaba los 1740.99 dólares la onza[28] A mediados de mayo la onza alcanza 1.911,56 dólares[29]
- El oro tocó su máximo histórico en agosto de 2020, cuando cotizó en 2.075 dólares, y con la invasión de Ucrania, en marzo de 2022, llegó hasta los 2.070 dólares.En abril de 2023 el precio de la onza de oro alcanza US $ 2 025[30] Su máximo histórico fue de 2.135,40 dólares el 4 de diciembre de 2023. cerró el año en 2.061,89 dólares la onza.[31]
- En septiembre de 2025 el precio del oro alcanzó un nuevo récord histórico al alcanzar los 3.751,02 dólares por onza troy.[32] En diciembre el oro subió a 4.420,30 dólares la onza.[33]
- En enero de 2026 el oro alcanzó los 4.600 dólares la onza un precio récord.[34]
Véase también
- Iridio
- Pepita de oro
- Patrón oro
- Reserva de oro
- Crisofobia
- Tejido de oro
- Lingote de oro
- Fiebre de oro
- Envenenamiento por mercurio
- Cloruro de oro(III)
Referencias
- ↑ Landau, Elizabeth (18 de julio de 2013). «Todo el oro del planeta provino de la colisión de estrellas de neutrones». cnn.com. Consultado el 21 de septiembre de 2018.
- ↑ a b «Metalurgia». Banco de la República de Colombia. 2008. Archivado desde el original el 19 de noviembre de 2012. Consultado el 19 de septiembre de 2010.
- ↑ a b Audi, G. (2003). «The NUBASE Evaluation of Nuclear and Decay Properties». Nuclear Physics A (Atomic Mass Data Center) 729: 3-128. ISSN 0375-9474. doi:10.1016/j.nuclphysa.2003.11.001.
- ↑ «La Caixa saca de un largo olvido al enigmático pueblo tracio». Terra. Archivado desde el original el 28 de junio de 2012. Consultado el 9 de mayo de 2010.
- ↑ «El Museo Museo Nacional del Indígena Americano del Smithsonian ha devuelto a Perú la conocida como Placa Echenique, una obra de orfebrería precolombina símbolo de la ciudad de Cuzco.» «EEUU devuelve a Perú la Placa Echenique, una obra de orfebrería precolombina». Europa Press. 20 de junio de 2021.
- ↑ «Una importante selección de piezas del Museo Oro del Perú ya están en Budapest y San Petersburgo. El Comercio acompañó el proceso de embalaje y traslado de estos invaluables objetos de la colección de Miguel Mujica Gallo» «¿Cómo viajan a Europa los tesoros culturales del Perú?». El Comercio. 18 de marzo de 2019.
- ↑ « Esta da pie a la gira internacional de una impresionante selección de 192 piezas provenientes de la famosa ciudadela, así como de tumbas reales de diversas culturas pre incas; pieza que pertenece a la cultura Mochica (1 dC - 800 dC). es el adorno frontal de un tocado de oro de 18 quilates. Representa la cabeza de felino con tocado de media luna y dos aves » «¿Qué emblemáticas piezas vinculadas a Machu Picchu y otras culturas pre incas se exhibirán en Florida desde octubre?». El Comercio. 25 de mayo de 2021.
- ↑ «los legendarios mochicas levantaron sus centros de poder y dejaron guardados como tesoros dos piezas de metal, el Tumi de Oro y la Máscara Sicán que hablan por sí solas de la calidad de los orfebres» «El Tumi de Oro y la Máscara Sicán valen un Perú». RPP Noticias. 26 de julio de 2017.
- ↑ « En 1937 Julio C. Tello recuperó, para el Museo Nacional, diversos objetos de oro y plata que provenían de la huaca ‘La ventana’, en Batán Grande, jurisdicción de Poma, en Lambayeque» «El Tumi de oro y el uso que tenía en el Perú antiguo». Trome. 6 de septiembre de 2016.
- ↑ http://oilprice.com/Metals/Gold/Gold-Mining-Boom-Increasing-Mercury-Pollution-Risk.html Gold Mining Boom Increasing Mercury Pollution Risk
- ↑ Messori, L.; Marcon, G. (2004). «Gold Complexes in the treatment of Rheumatoid Arthritis». En Sigel, Astrid, ed. Metal ions and their complexes in medication. CRC Press. pp. 280-301. ISBN 978-0-8247-5351-1.
- ↑ «El oro como valor refugio.»
- ↑ U.S. Geological Survey, [1]
- ↑ U.S. Geological Survey (Mineral Commodity Summaries). 2021. Oro, Revisado el 1 de abril de 2021.
- ↑ « » «China, Australia y Rusia produjeron el 31% del oro que se extrajo durante 2020». Oro Informacion. 26 de marzo de 2021.
- ↑ http://atlas.media.mit.edu/es/profile/hs92/7108/
- ↑ Koos, Carlo; Basedau, Matthias (2013-09). «Does Uranium Mining Increase Civil Conflict Risk? Evidence from a Spatiotemporal Analysis of Africa from 1960 to 2008». Civil Wars (en inglés) 15 (3): 306-331. ISSN 1369-8249. doi:10.1080/13698249.2013.842744. Consultado el 29 de febrero de 2024.
- ↑ «Conflict Minerals | Responsible Minerals | Global Witness». Global Witness (en inglés). Consultado el 15 de febrero de 2024.
- ↑ «Qué impacto tiene tu PC en el medio ambiente». Archivado desde el original el 7 de junio de 2019. Consultado el 7 de junio de 2019.
- ↑ Calabrese, Alberto I.; Astolfi, Emilio A. (enero de 1969). Toxicología. Buenos Aires, Argentina: Kapelusz. p. 147. OCLC 14501248.
- ↑ Tena, Alejandro (20 de noviembre de 2019). «El negocio del litio, el oro blanco de la nueva era energética». Público.
- ↑ «¿Qué es el oro laminado y cuál es su precio?». 6 de septiembre de 2018. Consultado el 7 de abril de 2020.
- ↑ Nota de prensa: El auge del compro oro
- ↑ «El precio del oro se da un batacazo: en un solo día cae a niveles de 1983.»
- ↑ « gráfica de 2013-2016 del precio del oro » «Cotización histórica del oro últimos 5, 10, 20 y 50 años». Preciodeloro. 14 de agosto de 2020.
- ↑ «20/05/2016: Oro pierde un 1,5% en la semana». BullionVault. 20 de mayo de 2016.
- ↑ « » «2020, el año del oro: tuvo su mejor rendimiento en una década y se prevé que su precio crezca más». Infobae. 31 de diciembre de 2020.
- ↑ « » «El oro se dirige a cerrar otra semana en alza tras la depreciación del dólar». Banca y Negocios. 19 de marzo de 2021.
- ↑ « » «Precio del oro supera los US$1.900 por onza por primera vez desde enero». Bancaynegocios. 26 de mayo de 2021.
- ↑ «El oro sube el 2% y cotiza en 2.025 dólares, máximos desde la invasión rusa». Banca y Negocios. 4 de abril de 2023. «El oro, explican los expertos, mantiene una correlación inversa con el dólar, aumentando o disminuyendo su valor dependiendo de la fortaleza de la divisa estadounidense».
- ↑ «El oro supera los US$ 2.000 y se encamina a su mejor año de los últimos tres». Finanzas Digital. 29 de diciembre de 2023.
- ↑ «Precio del oro sigue en alza: cotización superó máximo de US$3.750 por onza». Alberto News. 22 de septiembre de 2025.
- ↑ «Precio del oro marca récord por tensiones entre EE.UU. y Venezuela». Banca y Negocios. 22 de diciembre de 2026.
- ↑ «Dato: Precios del oro y de la plata baten récords tras investigación de la Reserva Federal de EEUU». Banca y Negocios. 12 de enero de 2026.
Bibliografía
- Cotton, F. A.; Wilkinson, G.; Murillo, C. A.; Bochman, M. Advanced Inorganic Chemistry, A comprehensive Text, 6.ª Ed., Wiley & Sons, 1999.
- Hans-Jürgen Quadbeck-Seeger(Ed.); Faust, Rüdiger; Knaus, Günter & Siemeling, Ulrich. World Records in Chemistry, Wiley-VCH, 1999.
- Holleman, A. F. & Wiberg, Egon. Inorganic Chemistry, Academic Press, 2001.
- Housecraft, C. E. & Sharpe, A. G. Química inorgánica, 2.ª edición, Pearson Prentice Hall, 2006.
- Wulfsberg, G. Inorganic Chemistry, 1.ª Ed., University Science Books, 2000.
_NIST_ASD_emission_spectrum.png)