Cobalto
| Hierro ← Cobalto → Níquel | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabla completa • Tabla ampliada | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Información general | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombre, símbolo, número | Cobalto, Co, 27 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie química | Metales de transición | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 9, 4, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atómica | 58,933200 u | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuración electrónica | [Ar] 3d7 4s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Mohs | 4,1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrones por nivel | 2, 8, 15, 2 (imagen) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | Metálico con tono gris | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio medio | 135 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegatividad | 1.88 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico (calc) | 152 pm (radio de Bohr) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | 126 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado(s) de oxidación | 5, 4 , 3, 2, 1, -1 (anfótero) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1.ª energía de ionización | 760,4 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.ª energía de ionización | 1648 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3.ª energía de ionización | 3232 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4.ª energía de ionización | 4950 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Líneas espectrales |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado ordinario | Sólido (ferromagnético) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad | 8900 kg/m3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de fusión | 1768 K (1495 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de ebullición | 3200 K (2927 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de vaporización | 376,5 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de fusión | 16,19 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presión de vapor | 175 Pa a 1768 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varios | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristalina | Hexagonal | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor específico | 420 J/(kg·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad térmica | 100 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidad del sonido | 4720 m/s a 293,15 K (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isótopos más estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Artículo principal: Isótopos del cobalto | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Valores en el SI y condiciones normales de presión y temperatura, salvo que se indique lo contrario. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El cobalto (del alemán kobalt, voz derivada de kobolds, los «Duendes» que, según los mineros de Sajonia de la Edad Media, eran espíritus de la tierra que tenían embrujado el mineral, por lo que, aunque parecía mena de cobre, no producía este elemento con el tratamiento habitual[1]) es un elemento químico de número atómico 27 y símbolo Co situado en el grupo 9 de la tabla periódica de los elementos.[2][3]
Su masa atómica es de 58,9332. Con propiedades magnéticas similares al hierro como su dureza, resistencia a la tensión y propiedades térmicas. El cobalto se puede encontrar en aguas dulces, suelos, plantas, meteoritos y en los nódulos de manganeso encontrados en el fondo del océano. Los compuestos de cobalto se usan para crear un color azul denso en vidrios, cerámicas, porcelanas, vidriar y en esmaltes.[4]
Algunas de sus características son: El número atómico es 27, su número de valencia es 2,3, el estado de oxidación es +3, su electronegatividad es 1,8, el radio covalente (Á) es 1,26, el radio iónico (Á) es 0,63, el radio atómico (Á) es 1,25, su configuración [Ar]3d⁷ 4s², su masa atómica (g/mol) es 58,93, su densidad (g/ml) es 8,9, el punto de ebullición (°C) es 2900, el punto de fusión (°C) es 1495.[4]
Etimología
Se le denominaba kobold en la Edad Media por los mineros que consideraban este metal sin valor y tenían la creencia de que un buen duende (un kobold) lo ponía en sustitución de la plata que había robado.[5] En el diccionario castellano del siglo XVIII aparece como cobalt.
Características principales

El cobalto es un metal ferromagnético, de color blanco azulado. Su temperatura de Curie es de 1388 K. Normalmente se encuentra junto con níquel, y ambos suelen formar parte de los meteoritos de hierro. Es un elemento químico esencial para los mamíferos en pequeñas cantidades. El Co-60, un radioisótopo de cobalto, es un importante trazador y agente en el tratamiento del cáncer.
El cobalto metálico está comúnmente constituido de una mezcla de dos formas alotrópicas con estructuras cristalinas hexagonal y cúbica centrada en las caras siendo la temperatura de transición entre ambas de 722 K.
Se emplea sobre todo en superaleaciones de alto rendimiento, siendo éstas normalmente más caras que las de níquel. Es un metal eminentemente de aleación, al igual que el níquel o el zinc, por ejemplo. Dichos metales suelen agregarse a otros que actúan de base, aunque cuando el cobalto actúa de base suele hacerlo en aleaciones con cromo. Su principal característica es su elevadísima dureza y resistencia al desgaste. Son aleaciones normalmente poco usadas ya que su virtud no compensa la gran cantidad que hay que abonar por ellas. El cobalto posee características muy similares a sus elementos vecinos, hierro y níquel, con los cuales comparte más rasgos que con los elementos de su propio grupo en la tabla periódica. Ni cobalto ni níquel suelen mezclarse con la plata ni el mercurio (siendo ambos raras excepciones) además de que comparten el efecto magnético del hierro. El cobalto es el metal más escaso de estos tres, es el menos rentable y también el más caro. Encuentra pocos usos en la industria en comparación a sus vecinos inmediatos. Se trata de uno de los pocos elementos químicos monoisotópicos. El cobalto tiene poca resistencia química aunque es más estable que el hierro ya que se mantiene en aire y agua siempre que no se encuentren otros elementos corrosivos en dichos medios.
Presenta estados de oxidación bajos. Los compuestos en los que el cobalto tiene un estado de oxidación de +4 son poco comunes. El estado de oxidación +2 es muy frecuente, así como el +3. También existen complejos importantes con el estado de oxidación +2.
Historia

Los compuestos de cobalto se han utilizado durante siglos para obtener un color azul intenso en el vidrio, esmaltes y cerámicas. Se ha detectado cobalto en esculturas egipcias y en joyas persas desde el tercer milenio a. C., en las ruinas de Pompeya (destruida en el año 79 d. C.), y en China, en la dinastía Tang (618-907 d. C.) y la dinastía Ming (1368-1644 d. C.).[6]
El cobalto se ha empleado para colorear el vidrio desde la Edad del Bronce. La excavación del naufragio Uluburun encontró un lingote de cristal azul, que fue confeccionado durante el siglo XIV a. C.[7][8] Artículos de cristal azul de Egipto son de color con el cobre, el hierro o el cobalto. El vaso más antiguo coloreado con cobalto es de la época de la dinastía XVIII de Egipto (1550-1292 a. C.). Se desconoce el lugar donde se obtuvieron los compuestos de cobalto.[9][10]
El elemento fue descubierto por el químico sueco George Brandt. La fecha del descubrimiento varía en las diversas fuentes entre 1730 y 1737. Mostrando que es un nuevo elemento hasta entonces desconocido diferente de bismuto y otros metales tradicionales, y decir que es un nuevo "semi-metal".[11][12] Brandt fue capaz de demostrar que el cobalto era el responsable del color azul del vidrio que previamente se atribuía al bismuto. El cobalto se convirtió en el primer metal descubierto desde la época prehistórica, en la que todos los metales conocidos (hierro, cobre, plata, oro, zinc, mercurio, estaño, plomo y bismuto) no tenían descubridores registrados.
Su nombre proviene del alemán kobalt de kobold, llamado así por los mineros por su color, toxicidad y los problemas que ocasionaba ya que al igual que el níquel contaminaba y degradaba los elementos que se deseaba extraer. Los primeros intentos de fundición de estas menas para obtener metales como el cobre o el níquel, fracasaban dando en su lugar simplemente un polvo (óxido de cobalto (II)). Además, debido a que los minerales primarios de cobalto siempre contienen arsénico, la fundición de estas menas oxidaba el contenido de arsénico para dar el altamente tóxico y volátil, óxido de arsénico, lo que también disminuye el aprecio de estas menas para los mineros.[13]
Durante el siglo XIX, una parte significativa de la producción mundial, entre el 70 y 80%, de azul cobalto (un tinte hecho con compuestos de cobalto y alúmina) y esmalte (vidrio de cobalto en polvo para uso con fines de pigmento en cerámica y pintura) se llevó a cabo en la fábrica noruega Blaafarveværket[14][15] adquirida en 1823 por el barón W. C. Benecke y el industrial prusiano Benjamin Wegner. Las primeras minas para la producción de esmalte entre los siglos XVI al XVIII se encontraban en Noruega, Suecia, Sajonia y Hungría. Con el descubrimiento de mineral de cobalto en Nueva Caledonia en 1864 la extracción de cobalto en Europa disminuyó. Con el descubrimiento de yacimientos minerales en Ontario, Canadá en 1904 y de yacimientos aún mayores en la provincia de Katanga en el Congo en 1914, las operaciones mineras cambiaron de nuevo.[13] Por el conflicto de Shaba a partir de 1978, la principal fuente de cobalto, las minas de cobre de la provincia de Katanga, casi detuvieron su producción.[16][17] El impacto en la economía mundial de cobalto de este conflicto fue menor de lo esperado, porque la industria establecida formas efectivas para reciclar de materiales de cobalto y en algunos casos fue capaz de cambiar a alternativas sin cobalto.[16][17]
En 1938 John Livingood y Glenn Seaborg descubrieron el cobalto-60.[18] La primera máquina de radioterapia, bomba de cobalto, construida en Canadá por un equipo liderado por Ivan Smith y Roy Errington se utilizó en un paciente el 27 de octubre de 1951; el equipo se encuentra actualmente expuesto en el Saskatoon Cancer Centre, en la ciudad de Saskatoon (Saskatchewan).
Después de la Segunda Guerra Mundial, los EE. UU. quería asegurase de que nunca le faltaría el mineral de cobalto necesario, como le había ocurrido a los alemanes y fue la exploración de una fuente dentro de la frontera de los EE. UU. Un buen suministro de los minerales necesarios se encuentra en Idaho cerca del cañón Blackbird en la ladera de una montaña. La Compañía Minera Calera comenzó la producción en este lugar[19]
La única refinería electrolítica de cobalto de Iberoamérica se encuentra en San Pablo, Brasil, y fue construida en 1981.[20]
Producción

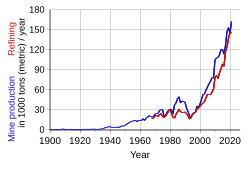
En 2005, los depósitos de cobre en la provincia de Katanga (antigua provincia de Shaba) de la República Democrática del Congo fueron el principal productor de cobalto con casi el 40% cuota mundial, según informa el Servicio Geológico Británico.[21] La situación política en el Congo influye en el precio de cobalto de manera significativa.[22]
La República Democrática del Congo es el mayor productor de cobalto. Según un informe de la revista especializada Illuminem, los principales productores son empresas con sede en Gran Bretaña (Glencore y Eurasian Natural Resources) y China (China Molybdenum y Metorex). Los accionistas chinos, a su vez, controlan las dos empresas, que representan el 13,8 % de la producción mundial y alrededor del 24 % de la producción de las empresas grandes, conocidas y activas. Por el contrario, las empresas con sede en la República Democrática del Congo controlan solo el 3,5 % de la producción mundial.[23]
El proyecto de la Montaña Mukondo, operado por la Central African Mining and Exploration Company (CAMEC) en Katanga, puede ser la más rica reserva de cobalto en el mundo. Se estima que será capaz de producir alrededor de un tercio de la producción total mundial de cobalto en el 2008.[24] En julio de 2009 CAMEC anunció un acuerdo a largo plazo en virtud del cual CAMEC entregaría toda su producción anual de concentrado de cobalto de la Montaña Mukondo a Zhejiang Galico Cobalt & Nickel Materials de China.[25]
Existen varios métodos para separar el cobalto del cobre y níquel. Dependen de la concentración de cobalto y la composición exacta del mineral utilizado. Una etapa de separación implica flotación por espuma, en el que los tensioactivos se unen a los diferentes componentes del mineral, dando lugar a un enriquecimiento de mena de cobalto. Tras el tostado se convierte la mena a sulfato de cobalto, mientras que el cobre y el hierro se oxida al óxido. La lixiviación con agua extrae el sulfato junto con los arseniatos. Los residuos están además lixiviado con ácido sulfúrico obteniéndose una solución de sulfato de cobre. El cobalto también puede ser lixiviado de la escoria de la fundición de cobre.[26]
Los productos de los procesos mencionados anteriormente se transforman en óxido de cobalto (Co3O4). Este óxido se reduce al metal por la reacción aluminotérmica o reducción con carbono en un alto horno.[27]
| 1. | 3.500.000 | |
| 2. | 1.400.000 | |
| 3. | 600.000 | |
| 4. | 500.000 | |
| 5. | 260.000 | |
| 6. | 250.000 | |
| 7. | 220.000 | |
| 8. | 100.000 | |
| 9. | 80.000 | |
| 10. | 69.000 | |
| 11. | 47.000 | |
| 12. | 13.000 |
Fuente: USGS
Aplicaciones

El cobalto suele usarse en diversas industrias y para muchas aplicaciones, como por ejemplo:[29]
- En la creación de muchas aleaciones para uso industrial
- Para la pigmentación permanente del cristal, la cerámica, la porcelana y otros trabajos artesanales
- Radiografía industrial para el control de calidad de metales (detección de grietas)
- Aleaciones entre las que cabe señalar superaleaciones usadas en turbinas de gas de aviación, aleaciones resistentes a la corrosión, aceros rápidos, y carburos cementados y herramientas de diamante. Herramientas de corte en procesos de fabricación para fresadoras.
- Imanes (Alnico, Fernico, Cunico, Cunife) y cintas magnéticas.
- Catálisis del petróleo e industria química.
- Recubrimientos metálicos por deposición electrolítica por su aspecto, dureza y resistencia a la oxidación.
- Secante para pinturas, barnices y tintas.
- Recubrimiento base de esmaltes vitrificados.
- Pigmentos (cobalto azul y cobalto verde).
- Electrodos de baterías eléctricas
- Cables de acero de neumáticos.
- El Co-60 se usa como fuente de radiación gamma en radioterapia, esterilización de alimentos (pasteurización fría) y radiografía industrial para el control de calidad de metales (detección de grietas).
Compuestos
Debido a los varios estados de oxidación que presenta, existe un abundante número de compuestos de cobalto. Los óxidos CoO (temperatura de Néel 291 K) y Co3O4 (temperatura de Néel 40 K) son ambos antiferromagnéticos a baja temperatura.
Isótopos

Se han caracterizado 22 radioisótopos siendo los más estables el Co-60, el Co-57 y el Co-56 con periodos de semidesintegración de 5,2714 años, 271,79 días y 70,86 días respectivamente. Los demás isótopos radiactivos tienen periodos de semidesintegración inferiores a 18 horas y la mayoría menores de 1 segundo. El cobalto presenta además cuatro metaestados, todos ellos con periodos de semidesintegración menores de 15 minutos.
La masa atómica de los isótopos del cobalto oscila entre 50 uma (Co-50) y 73 uma (Co-73). Los isótopos más ligeros que el estable (Co-59) se desintegran principalmente por captura electrónica originando isótopos de hierro, mientras que los más pesados que el isótopo estable se desintegran por emisión beta dando lugar a isótopos de níquel.
El cobalto-60 se usa en radioterapia en sustitución del radio por su menor precio (y considerando que el radio se desintegra en radón que es un elemento radiactivo y se presenta en forma de gas, por lo que es difícil encapsularlo para evitar contaminación radiactiva). Produce dos rayos gamma con energías de 1,17 MeV y 1,33 MeV y al ser la fuente empleada de unos dos centímetros de radio provoca la aparición de zonas de penumbra dispersando la radiación en torno a la dirección de radiación. El metal tiende a producir un polvo muy fino que dificulta la protección frente a la radiación. La fuente de Co-60 tiene una vida útil de aproximadamente 5 años, pero superado ese tiempo sigue siendo muy radiactivo, por lo que estas fuentes han perdido, en cierta medida, su popularidad en occidente.
Función biológica
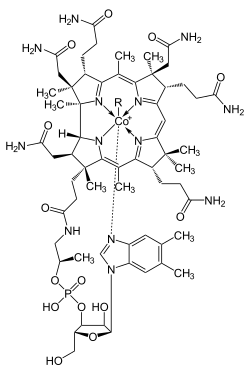
El cobalto es esencial en todos los animales, incluyendo los humanos. Forma parte de la cobalamina (vitamina B12). Una deficiencia de cobalto puede llevar a anemia. Pese a ello, la anemia secundaria por déficit de cobalto es muy rara, debido a que basta con consumir trazas del elemento para mantener la correcta homeostasis. Además, el cobalto es un elemento que se encuentra en varios alimentos, siendo difícil un déficit por baja ingesta.
Las proteínas basadas en la cobalamina usan el anillo de corrina para mantener unido el cobalto. La coenzima B12 proporciona el enlace C-Co, el cual participa en las reacciones.
Precauciones
El cobalto metálico en polvo finamente dividido es inflamable. Los compuestos de cobalto en general deben manipularse con precaución por la ligera toxicidad del metal.
El Co-60 es radiactivo y la exposición a su radiación puede provocar cáncer. La ingestión de Co-60 conlleva la acumulación de alguna cantidad en los tejidos, cantidad que se elimina muy lentamente. En una eventual confrontación nuclear, la emisión de neutrones convertiría el hierro en Co-60 multiplicando los efectos de la radiación tras la explosión y prolongando en el tiempo los efectos de la contaminación radioactiva; con este propósito se diseñan algunas armas nucleares denominadas bombas sucias (del inglés dirty bomb). En ausencia de guerra nuclear, el riesgo proviene de la inadecuada manipulación o mantenimiento de las unidades de radioterapia.
Además al respirar elevadas cantidades de cobalto podemos llegar a experimentar problemas en los pulmones como asma y neumonía esto ocurre más en las personas que trabajan con el cobalto.
Los alimentos que tengas partículas de cobalto también pueden llegar a dañarnos especialmente los vegetales que crezcan a partir de suelos contaminados con estas partículas, esto puede traer grandes efectos en nuestra salud como por ejemplo:[4]
- Vómitos y náuseas
- Problemas de visión
- Problemas del corazón
- Daño de la tiroides
Cobalto en la tecnología
El cobalto contiene características de estabilidad, dureza, anticorrosión y resistencia a altas temperaturas que lo hace ideal para el desarrollo tecnológico como la producción de dispositivos electrónicos que usamos diariamente como los teléfonos inteligentes, computadores o tabletas.
La función del cobalto en la tecnología es que en las baterías que se construyen con el cobalto se utiliza el componente de electrodo positivo (cátodo) y electrodo negativo (ánodo) esto puede ser gracias al grafito o al carbón. Gracias al cobalto se puede alcanzar un rendimiento de capacidad de almacenamiento tres veces mayor a las baterías que no utilizan el cobalto en su fabricación. Gracias al cobalto se busca potenciar el rendimiento del litio en las baterías que usamos en los dispositivos electrónicos diarios aumentando su autonomía.
A medida que avanzamos hacia un futuro de cero emisiones de gases de efecto invernadero, las baterías a base de cobalto serán cada vez más solicitadas para ayudar a “descarbonizar” estos componentes y ayudar a integrar la energía renovable en las redes eléctricas.[30]
Uno de los problemas del cobalto es que la mayoría de los vehículos eléctricos dependen de grandes baterías de iones de litio, esto trae la duda sobre la continuidad del suministro mundial del metal. A pesar de eso, el cobalto es uno de los elementos con mayor inquietud. Olivetti científica confirma que los mejores cátodos de las baterías de litio contienen cobalto y su producción es escasa, por ende, se calcula que ocurrirá lo mismo con el suministro de cobalto si los coches eléctricos fueran tan conocidos como se espera y sus resultados no son confortadores. El cátodo de las baterías de litio forman una combinación de cobalto y otros metales. Las propiedades atómicas de este elemento permiten que el cátodo guarde una gran cantidad de energía en poco espacio y ayudan a conservar su forma laminar. El cobalto es un subproducto de la minería de cobre y níquel, de manera que su producción depende de la demanda de esos metales. También, más de la mitad del cobalto del planeta se halla en la inestable República Democrática del Congo. Reutilizar baterías de litio es sumamente difícil, apenas se lleva a cabo. Pero incluso con mayores tasas de reciclado y procesos más económicos. Gaines, analista de sistemas, asegura que “el reciclaje no tendrá un impacto significativo hasta diez o más años después de la introducción en masa de los vehículos eléctricos”. Varios prototipos recientes con alto contenido en níquel reducirían la demanda de cobalto. Los investigadores esperan hacer más práctico el desarrollo de cátodos sin cobalto.[31]
El cobalto se utiliza también en imanes de ferrita, conocidos como imanes de cerámica, junto con otros metales como el óxido de hierro y varios metales. Estos imanes se usan en radios, altavoces, microondas, relés, discos, motores de imán permanente y la cinta magnética, para almacenar información.
Otros imanes que utilizan cobalto son los imanes de alnico, formado por aluminio y níquel. Estos ofrecen una buena resistencia magnética y soportan temperaturas de hasta 425 °C. Se usan en motores eléctricos, pastillas de guitarras eléctricas, cojinetes y acoplamientos magnéticos, sistemas ABS y en aplicaciones militares y aeroespaciales. Debido a su sensibilidad a la desmagnetización, la forma y la longitud son fundamentales.
Actualmente este tipo de superaleaciones, así como para ciertas aleaciones cerámicas y cobalto, se abre camino en el campo tecnológico de fabricación de vehículos aeroespaciales o estaciones orbitales.[32]
Situación en Argentina
En Argentina se descubrió una nueva especie para la ciencia, la cobaltomenita o también se le llamó en Argentina como cobalto criollo. Descubierto por el francés Emile Bertrand en el depósito selenifero de Cacheuta en Mendoza. Esto se obtiene a través de un subproducto del procesamiento de minerales de cobre y níquel.[33]
Argentina cuenta con grandes yacimientos de cobalto y otros materiales como las Águilas (San Luis), King tut (La Rioja) y La Niquelina-Esperanza (Salta).[34]
El cobalto en Argentina está tomando un rol muy importante en la medicina y también en el campo, principalmente en los alimentos. Dioxitek es una empresa estatal manejada por la Secretaría de Energía y por la CNEA(Comisión Nacional de Energía Atómica),la cual se dedica a la producción de polvo de dióxido de uranio que después es utilizado como combustible en las centrales nucleares de Atucha I, ubicada en el partido de Zárate y Embalse, en la provincia de Córdoba. Es la principal productora de cobalto-60 y una de las únicas productoras y abastecedoras en el mercado internacional. Convirtiendo así a Argentina en uno de los principales exportadores de cobalto-60 en el mercado internacional. Gracias a las ventas que obtuvo Dioxitek exportando obtuvo grandes ganancias logrando así invertir en tecnología para el desarrollo de la planta de fuentes selladas, la compra de equipamiento a nivel local y la concreción de otras inversiones proyectadas.
El cobalto-60 es muy importante en el campo, ya que se utiliza para la preservación de alimentos. El beneficio de usar este en los alimentos es higiénico, no tendrían la necesidad de usar fumigantes, conservantes químicos o sustancias que puedan perder la calidad de frescura del producto. Por esto el usar este en los alimentos que Argentina exporta al exterior incrementa su valor en el mercado.[35]
Lejos aún de que llegue una revolución en el mundo de las baterías para dispositivos electrónicos, seguimos viviendo de cerca la guerra de los fabricantes por conseguir el suministro de algunos de los materiales presentes en ellas. Si bien el litio es uno de los que más presencia tienen en el planeta, otros como el cobalto, son mucho más escasos y en consecuencia, se encarece su adquisición a medida que crece la demanda.
Sin embargo, el aumento en la demanda de estos materiales es algo relativamente reciente, infundado por el crecimiento del mercado del coche eléctrico y sobre todo por sus previsiones de seguir creciendo. El precio del cobalto ha crecido un 235% en 2017, pasando de 34.600 dólares por tonelada a 81.360 dólares.
En la actualidad, cada coche eléctrico requiere entre ocho y doce kilos de cobalto (frente a los ocho gramos que necesita la batería de un móvil), por lo que si se cumplen las estimaciones, se demandarán 200.000 toneladas de cobalto más cada año.[28]
Con todo, se puede ver que la demanda de cobalto, por lo menos a corto plazo, no va a hacer otra cosa que crecer. La situación en 2020, resultó en que, Argentina exportó $767 en cobalto, convirtiéndose en el exportador N°87 de cobalto en el mundo. Habiendo sido el producto número 1050 más exportado en Argentina. Siendo Francia ($767) el principal destino de estas exportaciones; e importó $1,18M en cobalto, convirtiéndose en el importador número 52 de cobalto en el mundo. Siendo el cobalto, el producto N°805 más importado en Argentina.[36]
Véase también
- Cobalto-60
Referencias
- ↑ Asimov, I. (2014). Breve historia de la química: Introducción a las ideas y conceptos de la química. Madrid: Alianza Editorial/El Libro de Bolsillo, p. 73.
- ↑ Garritz, Andoni (1998). Química. Pearson Educación. p. 856. ISBN 978-9-68444-318-1.
- ↑ Parry, Robert W. (1973). Química: fundamentos experimentales. Reverte. p. 703. ISBN 978-8-42917-466-3.
- ↑ a b c «Cobalto - Co».
- ↑ Breve diccionario etimológico de la lengua castellana, Joan Corominas, Madrid, Gredos, 1961.
- ↑ Cobalt, Encyclopædia Britannica Online.
- ↑ Pulak, Cemal (1998). «The Uluburun shipwreck: an overview». International Journal of Nautical Archaeology 27 (3): 188-224. doi:10.1111/j.1095-9270.1998.tb00803.x.
- ↑ Henderson, Julian (2000). «Glass». The Science and Archaeology of Materials: An Investigation of Inorganic Materials. Routledge. p. 60. ISBN 978-0-415-19933-9.
- ↑ Rehren, Th. (2003). «Aspects of the Production of Cobalt-blue Glass in Egypt». Archaeometry 43 (4): 483-489. doi:10.1111/1475-4754.00031.
- ↑ Lucas, A. (2003). Ancient Egyptian Materials and Industries. Kessinger Publishing. p. 217. ISBN 978-0-7661-5141-3.
- ↑ Georg Brandt first showed cobalt to be a new metal in: G. Brandt (1735) "Dissertatio de semimetallis" (Dissertation on semi-metals), Acta Literaria et Scientiarum Sveciae (Journal of Swedish literature and sciences), vol. 4, pages 1–10.
See also: (1) G. Brandt (1746) "Rön och anmärkningar angäende en synnerlig färg — cobolt" (Observations and remarks concerning an extraordinary pigment — cobalt), Kongliga Svenska vetenskapsakademiens handlingar (Transactions of the Royal Swedish Academy of Science), vol.7, pages 119–130; (2) G. Brandt (1748) “Cobalti nova species examinata et descripta” (Cobalto, a nuevo elemento examinado y descrito), Acta Regiae Societatis Scientiarum Upsaliensis (Journal of the Royal Scientific Society of Uppsala), 1st series, vol. 3 , pages 33–41; (3) James L. Marshall and Virginia R. Marshall (Spring 2003) "Rediscovery of the Elements: Riddarhyttan, Sweden," The Hexagon (official journal of the Alpha Chi Sigma fraternity of chemists), vol. 94, no. 1, pages 3–8. - ↑ Wang, Shijie (2006). «Cobalt—Its recovery, recycling, and application». Journal of the Minerals, Metals and Materials Society 58 (10): 47-50. Bibcode:2006JOM....58j..47W. doi:10.1007/s11837-006-0201-y.
- ↑ a b Dennis, W. H (2010). «Cobalt». Metallurgy: 1863–1963. pp. 254-256. ISBN 978-0-202-36361-5.
- ↑ Ivar B. Ramberg (2008). The making of a land: geology of Norway. Geological Society. pp. 98-. ISBN 978-82-92394-42-7. Consultado el 30 de abril de 2011.
- ↑ Cyclopaedia (1852). Cyclopædia of useful arts & manufactures, ed. by C. Tomlinson. 9 divs. pp. 400-. Consultado el 30 de abril de 2011.
- ↑ a b Wellmer, Friedrich-Wilhelm; Becker-Platen, Jens Dieter. «Global Nonfuel Mineral Resources and Sustainability». United States Geological Survey.
- ↑ a b Westing, Arthur H; Stockholm International Peace Research Institute (1986). «cobalt». Global resources and international conflict: environmental factors in strategic policy and action. pp. 75-78. ISBN 978-0-19-829104-6.
- ↑ Livingood, J.; Seaborg, G. (1938). «Long-Lived Radio Cobalt Isotopes». Physical Review 53 (10): 847. Bibcode:1938PhRv...53..847L. doi:10.1103/PhysRev.53.847.
- ↑ "Richest Hole In The Mountain" Popular Mechanics, May 1952, pp. 65–69.
- ↑ «Metalurgica em S. Miguel Paulista voltará a operar». Brasil Mineral (en portugués) (San Pablo). 2 de mayo de 2022. Consultado el 6 de octubre de 2022.
- ↑ «African Mineral Production». British Geological Survey. Consultado el 6 de junio de 2009.
- ↑ Wellmer, Friedrich-Wilhelm; Becker-Platen, Jens Dieter. «Global Nonfuel Mineral Resources and Sustainability». Consultado el 16 de mayo de 2009.
- ↑ Adnan Mazarei. «Who controls the world’s minerals needed for green energy?». illuminem (en inglés).
- ↑ «CAMEC – The Cobalt Champion». International Mining. julio de 2008. Consultado el 18 de noviembre de 2011.
- ↑ Amy Witherden (6 de julio de 2009). «Daily podcast – July 6, 2009». Mining weekly. Consultado el 15 de noviembre de 2011.
- ↑ Davis, Joseph R. (2000). ASM specialty handbook: nickel, cobalt, and their alloys. ASM International. p. 347. ISBN 0-87170-685-7.
- ↑ Holleman, A. F., Wiberg, E., Wiberg, N. (2007). «Cobalt». Lehrbuch der Anorganischen Chemie, 102nd ed. (en alemán). de Gruyter. pp. 1146–1152. ISBN 978-3-11-017770-1.
- ↑ a b «A por el oro azul: la guerra del cobalto ya no es solo cuestión de los grandes fabricantes de teléfonos o coches».
- ↑ «El cobalto, sus usos, propiedades e historia».
- ↑ «¿Cuál es la importancia del cobalto en la tecnología?».
- ↑ «El problema del cobalto».
- ↑ «El papel de los imanes en la industria y todas sus aplicaciones».
- ↑ «Cobalto: nuevo metal de moda».
- ↑ «“Conocer la potencialidad geológica de los elementos críticos es uno de los desafíos que tiene el Estado y la industria”».
- ↑ «Exportamos cantidad récord de Cobalto-60».
- ↑ «Cobalto en Argentina».
Enlaces externos
 Wikimedia Commons alberga una galería multimedia sobre Cobalto.
Wikimedia Commons alberga una galería multimedia sobre Cobalto.- ATSDR en español - ToxFAQs™: cobalto
- Enciclopedia Libre - Cobalto
- EnvironmentalChemistry.com - Cobalto
- Los Álamos National Laboratory - Cobalto
- WebElements.com - Cobalto
- La Química de Referencia - Cobalto
_NIST_ASD_emission_spectrum.png)